
8月9日,恒瑞医药发布公告称,该公司有多款创新药获批临床,其中包括多款抗肿瘤新药以及炎症性疾病、自身免疫性疾病新药。此外,近期有3款1类新药首次获批IND,它们均用于治疗实体瘤。
3款癌症1类新药首次获批IND
HRS-4508片是一款化药1类新药,为一种新型、高效、选择性的酪氨酸激酶抑制剂,通过抑制肿瘤细胞增殖发挥抗肿瘤作用。恒瑞医药公告未披露该药物的具体靶点,但指出中国暂无同类产品获批上市。
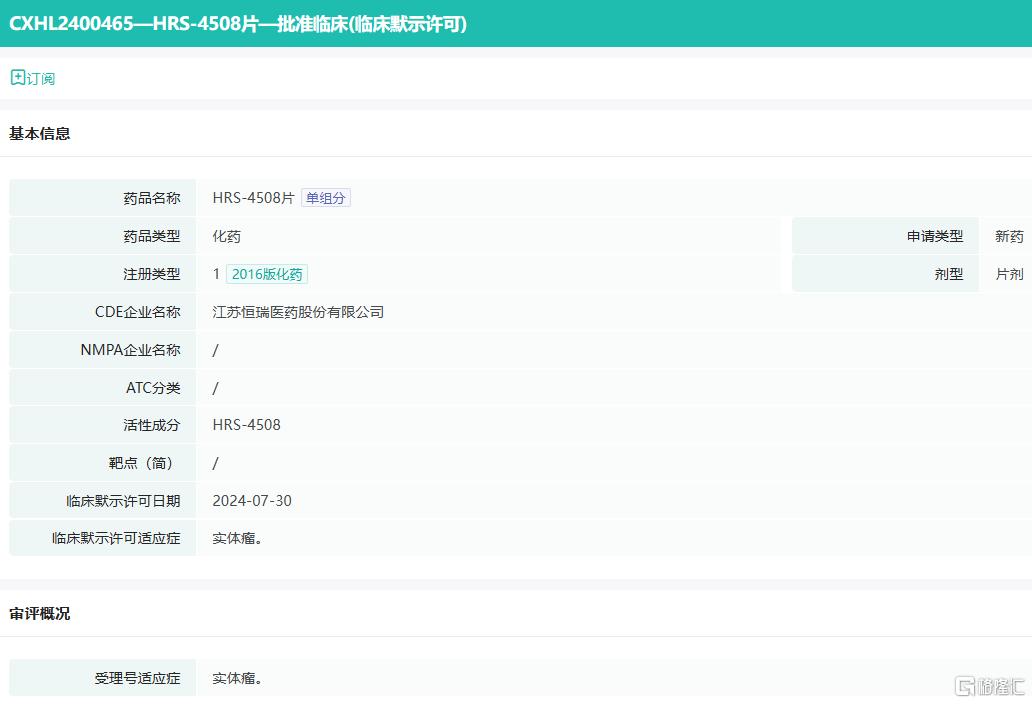 来源:药融云中国药品审评数据库
来源:药融云中国药品审评数据库
SHR-3821注射液是恒瑞医药自主研发的人源化抗体药物,拟用于治疗晚期恶性实体肿瘤,能够通过在肿瘤组织中特异性激活免疫细胞,发挥特异性抗肿瘤作用。恒瑞医药公告未披露该药物的具体靶点,但指出,目前中国暂无同靶点药物获批上市,数个同类药物处于临床开发阶段,适应症以晚期恶性肿瘤为主。
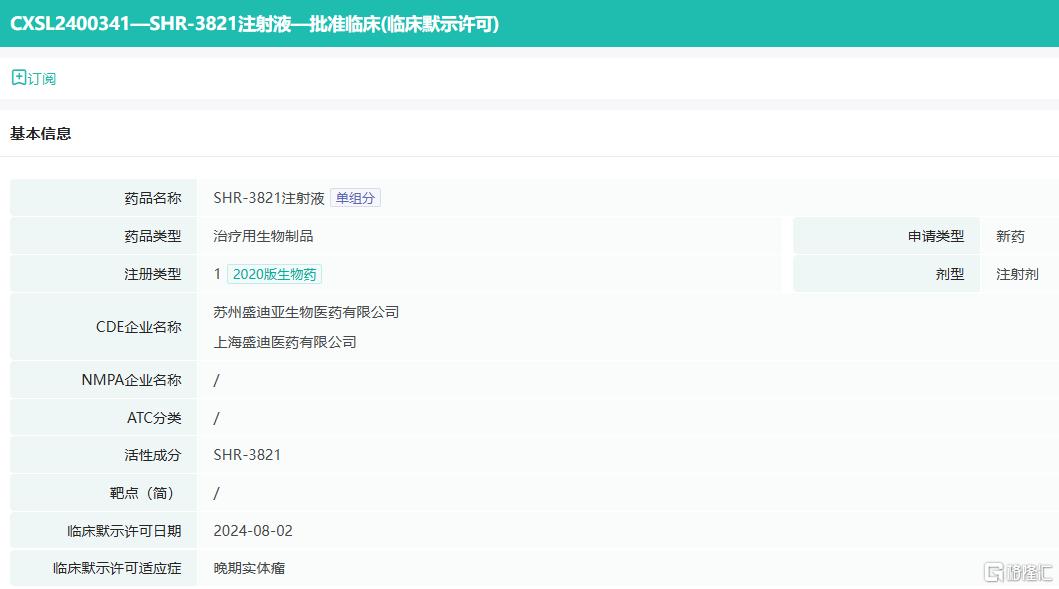 来源:药融云中国药品审评数据库
来源:药融云中国药品审评数据库
SHR-7787注射液为1类治疗用生物制品,通过诱导激活T细胞,使其发挥靶向杀伤恶性实体肿瘤细胞的作用。同样的,恒瑞医药公告尚未披露该药物的具体靶点,但指出目前中国尚无同类药物获批上市。
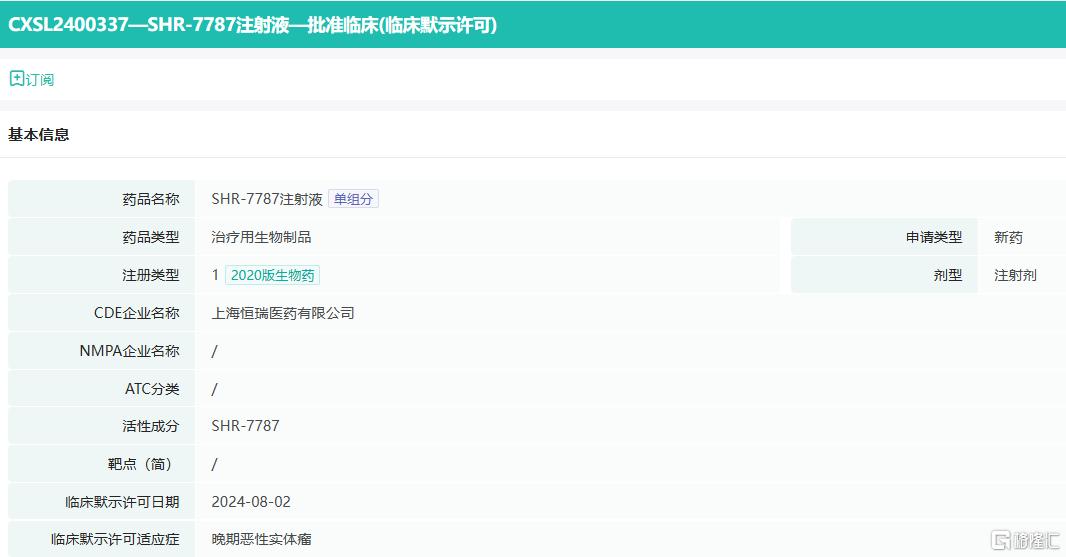 来源:药融云中国药品审评数据库
来源:药融云中国药品审评数据库
两款1类创新药获批3期临床
除了上述抗肿瘤新药,恒瑞医药还有两款在研1类新药获批3期临床研究,分别为SHR-1819注射液和夫那奇珠单抗注射液。
SHR-1819注射液是恒瑞医药自主研发的一种靶向人IL-4Rα的重组人源化单克隆抗体,能够同时阻断IL-4和IL-13的信号传导,拟用于治疗2型炎症相关疾病。该产品获批开展用于结节性痒疹(PN)患者的2/3期临床试验。
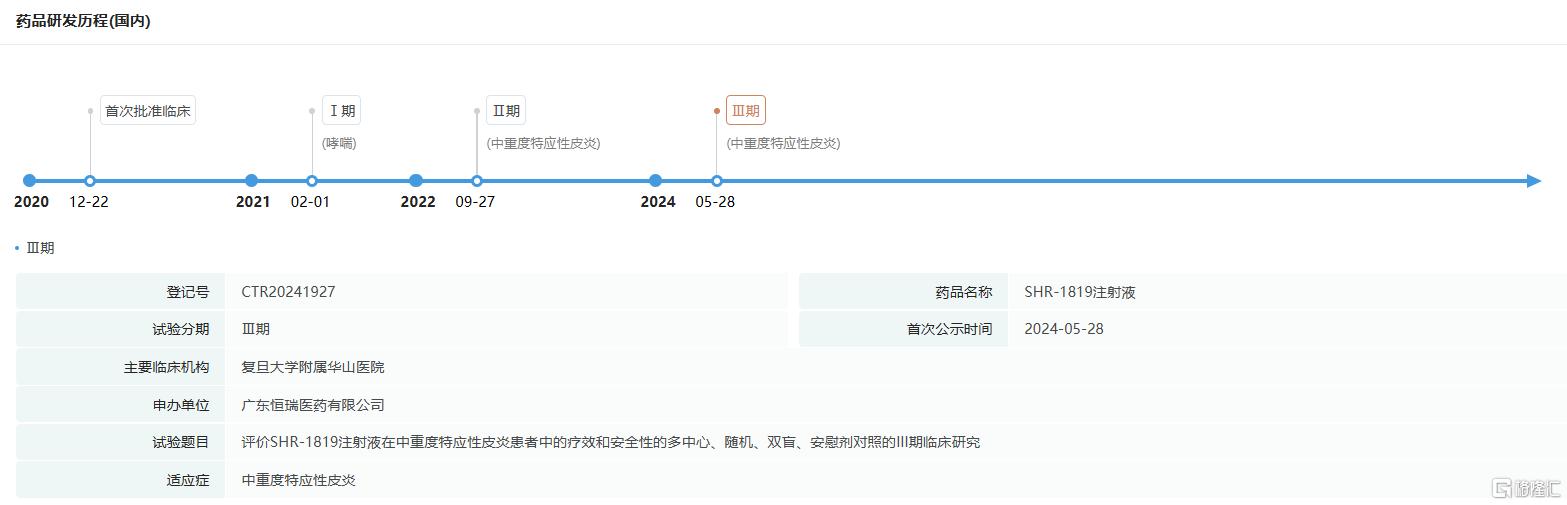 来源:药融云全球药物研发数据库
来源:药融云全球药物研发数据库
PN是一种慢性、炎症性皮肤疾病,临床特征为发作性的剧烈瘙痒和多发性结节损害。PN导致患者出现面临明显的生活质量下降、睡眠质量降低以及焦虑、抑郁等心理障碍问题。上皮衍生的细胞因子在PN的抓挠中不断释放,导致PN病变中的IL-4和其他2型细胞因子上调,从而进一步地促进炎症反应。与健康人相比,PN患者的IL-13 血浆水平也升高。IL-4Rα可控制IL-4及IL-13的信号传导,对引发2型炎症至关重要,是一种经充分验证的广泛作用靶点。
夫那奇珠单抗注射液获批开展3期临床试验,适应症为用于治疗适合接受系统治疗或光疗的6至小于18岁儿童和青少年中重度斑块状银屑病患者。
 截图来源:企业公告
截图来源:企业公告
夫那奇珠单抗是恒瑞医药自主研发的一种靶向人IL-17A的重组人源化单克隆抗体,拟用于治疗与IL-17通路相关的自身免疫疾病。该产品用于治疗中重度斑块状银屑病成人患者及活动性强直性脊柱炎成人患者适应症的上市申请已获受理。
据悉,基于夫那奇珠单抗在成人中重度斑块状银屑病中的疗效和安全性,恒瑞医药计划开展在6至小于18岁儿童和青少年中重度斑块状银屑病患者中的疗效和安全性研究。
参考来源:
[1] 药融云数据库
[2] 恒瑞医药官方公告
<END>
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员



