
细胞与基因治疗(CGT)是利用细胞和基因技术来治疗或预防疾病的新型生物医学手段,作为生物医药领域的前沿技术,近年来在全球范围内受到了广泛的关注。
最新的研究表明,CGT技术在治疗遗传性疾病、癌症和某些病毒感染性疾病中显示出较好的临床前景,特别是在癌症、罕见病等领域有着显著的应用潜力。随着技术的不断进步和临床应用的拓展,CGT领域正以前所未有的创新活力蓬勃发展。
本文基于药融咨询《CGT产业现状与未来趋势蓝皮书》中的部分内容,对CGT领域的创新趋势进行深度剖析,同时探讨其在拓宽适应症、革新治疗策略以及优化成本控制与支付模式等方面所取得的最新进展,为读者提供一个全面且深入的视角。
一、CGT应用领域不断拓宽:向实体瘤、传染病、慢性病扩大
CGT应用领域从罕见病和血液瘤向实体瘤、传染病、慢性病扩大。CGT的潜力正被不断挖掘,从最初聚焦于遗传性罕见病和血液瘤,如血友病、脑白质营养不良和B细胞淋巴瘤,到现在已逐步向实体瘤、慢性疾病及传染病等领域挺进。
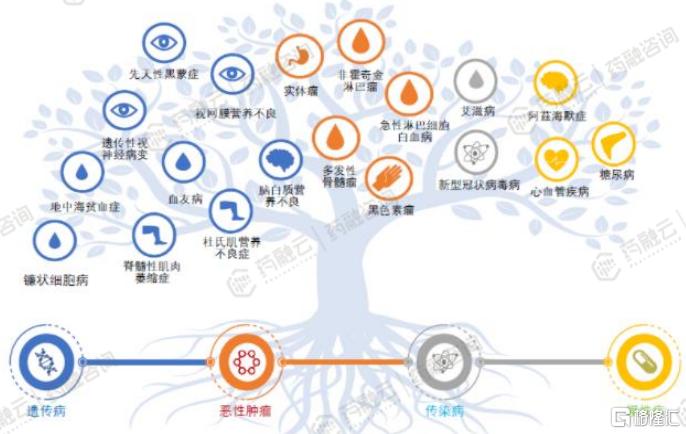
全球及中国在研的基因治疗临床试验中,肿瘤与感染性疾病的占比显著,预示着CGT的应用边界正在被不断拓宽。例如,针对糖尿病、心血管疾病等慢性疾病,以及艾滋病等传染病的治疗探索,正成为研究热点,标志着CGT正朝着多元化治疗领域迈进。
二、CGT治疗策略的革新:通用型、多靶点与联合疗法
1. CGT行业发展挑战
虽然细胞与基因治疗展现出巨大的治疗潜力,但要真正实现其广泛的应用和商业潜力,还需克服诸多挑战,不断推进技术创新、优化法规环境、降低生产成本、建立合理的支付机制,并妥善解决伦理和社会接受度问题。
(1)有效性挑战
①靶向递送效率:确保治疗基因或细胞精确到达并作用于目标细胞或组织是关键。当前,高效且特异性的递送系统仍然是一个挑战,尤其是对于非分裂细胞或深部组织的靶向。
②持久性与表达控制:在某些情况下,基因疗法需要长期稳定的基因表达以维持治疗效果,而在其他情况下,则可能需要可控的基因开关来调节治疗活性,这要求精确的基因调控机制。
③免疫反应:患者对转基因细胞或载体的免疫排斥反应可能影响治疗的有效性,需要通过策略来减少或管理这种反应。
(2)安全性挑战
①脱靶效应:基因编辑技术如CRISPR可能会导致非目标基因的意外编辑,引发潜在的安全问题,需要更加精准和特异的编辑工具。
②致癌风险:基因插入可能会激活原癌基因或干扰肿瘤抑制基因,增加患癌风险,需要在治疗前进行充分的风险评估。
③长期副作用:由于CGT的长期效果尚不完全清楚,长期监测和研究是必要的,以确保没有未预见的健康后果。
(3)成本挑战
①高昂的治疗费用:CGT的个性化定制、复杂的生产流程和严格的质量控制导致治疗成本极高,使得大多数患者难以承受。
②规模化生产难题:细胞与基因治疗产品的生产往往需要高度定制化,难以实现传统药物那样的大规模生产效率,增加了成本。
③支付与报销机制:现有的医疗保险和报销体系尚未充分适应CGT的高成本特性,如何建立合理的支付模型以确保患者可及性是一大难题。
(4)伦理与社会接受度
①伦理考量:基因编辑、细胞治疗等技术触及人类遗传物质,引发了关于基因隐私、基因编辑婴儿等伦理问题的广泛讨论。
②公众认知:提高公众对CGT技术的理解和信任,减少误解和恐惧,是推动该领域健康发展的重要一环。
③
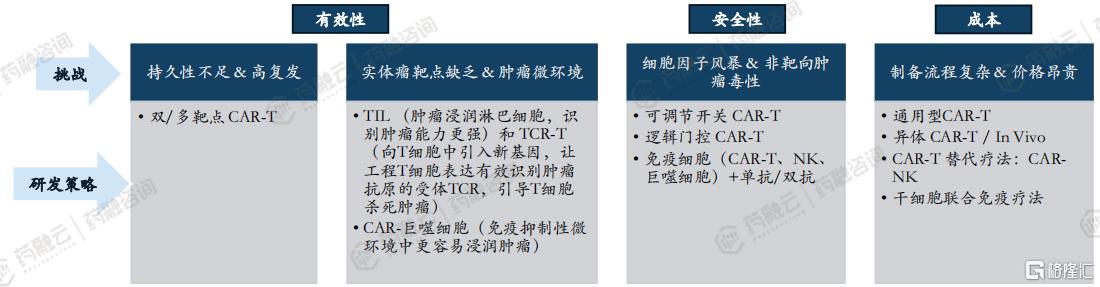
2. CGT研发策略
在细胞治疗领域,通用型CAR-T、多靶点CAR-T以及免疫细胞联合疗法等创新技术不断涌现。
通用型CAR-T(UCAR-T):具有工业化批量生产、周期短、成本低等优势,能够解决定制CAR-T的种种问题,如脱靶毒性、细胞因子风暴等安全性问题,以及制备工艺复杂、T细胞衰竭、适应症局限和费用昂贵等问题。通用型CAR-T的出现将极大地推动CAR-T疗法的普及和应用。
多靶点CAR-T:能有效避免因抗原逃逸引起的肿瘤复发,改善细胞治疗效率。针对多个靶点,多靶点CAR-T能够克服单一靶点容易丢失、反应下降、异质细胞负面影响等问题,提高治疗效果。
免疫细胞联合疗法:将免疫细胞(如CAR-T、NK、巨噬细胞)与单抗/双抗相结合,大幅提升抗癌效率。此外,干细胞联合免疫疗法也展现出巨大的潜力,通过将体外干细胞分化培养成CAR-T、NK、DC等免疫细胞,再回输病人体内,实现大规模量产、降低成本,并减少患者自体细胞提取生产的步骤。
三、成本降低与创新支付模式的齐头并进
面对CGT高昂的治疗费用,降低成本与创新支付模式成为行业内外共同努力的方向:
1. CGT成本降低路径
(1)通用型CAR-T可将耗材总成本从6万美元降为2000美元,将QC费用从3万美元降为1000美元,从而将生产成本从定制CAR-T的95780美元降低至4460美元。
(2)干细胞联合免疫疗法也能实现大规模量产、降低成本。
(3)CRO/CDMO也能有效降低成本。
2. 探索针对CGT创新支付体系
(1)美国已出台CAR-T疗法相关的支付政策,2021年提案将CAR-T细胞治疗产品纳入DRG打包支付,创建新的MS-DRG,利用DRG付费“结余留用,超额自负”的作用机制,有效控制CAR-T产品治疗费用,减轻患者负担。
(2)日本,CAR-T疗法的支付模式根据患者的年龄和临床收益,在医保支付的基础上,患者自付10%-30%,具体的支付数额可以降到41万日元左右。
(3)截至目前,国内已有5款CAR-T获批上市,福可苏(BCMA)价格高达116.6万元/针,靶向为CD19的奕凯达®、倍诺达®、源瑞达®价格分别高达120万元/针、129万元/针、99.9万元/针,都还未能进入医保目录,CAR-T疗法真正落实到患者仍任重道远。
国内获批上市的CAR-T疗法信息查询
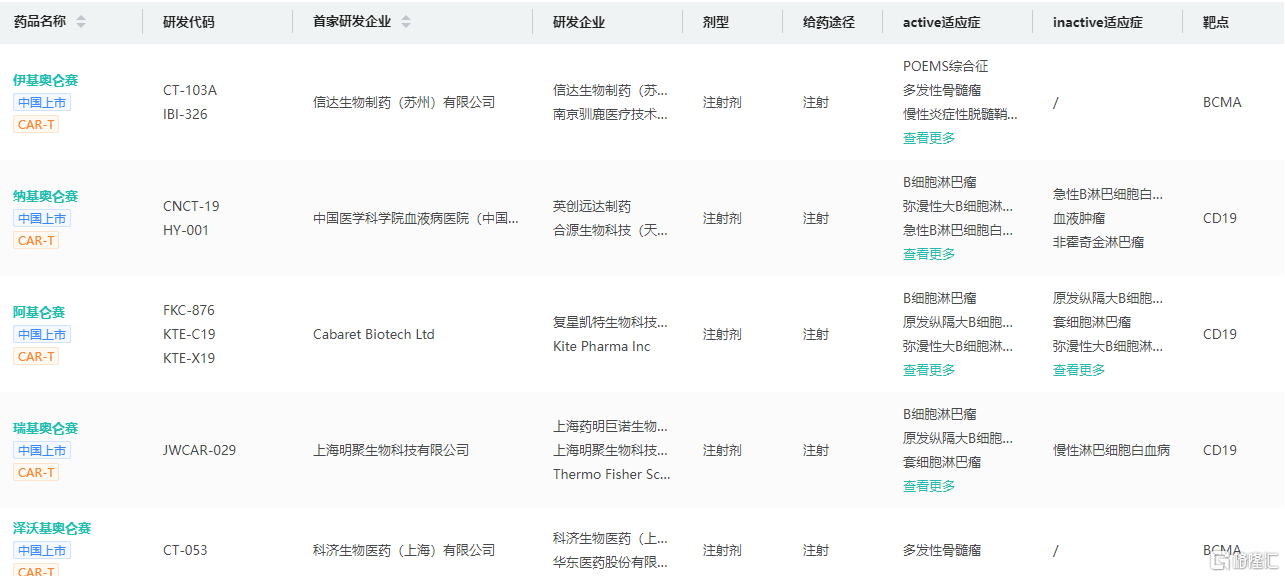
图片来源:药融云全球药物研发数据库
(4)目前商业保险,如太平人寿、平安人寿、新华、众安等保险机构纷纷将CAR-T疗法纳入了保障范围,同时百万医疗可以报销CAR-T疗法药物,比如惠民保,也有百万医疗险、高端医疗险、特药险等。复星凯特和药明巨诺、信达生物/驯鹿生物都在医保之外另辟蹊径,积极尝试各种创新支付方式来解决支付难题,提高药物可及性。
结语:
CGT领域正经历着一场深刻的变革,从治疗领域的拓展、治疗策略的革新,到成本控制与支付模式的创新,每一步进展都预示着这一前沿技术正逐步走向成熟,为更多患者带来治愈的曙光。未来,随着技术的不断突破和政策环境的持续优化,CGT有望开启精准医疗的新纪元,成为人类对抗疾病的重要武器。
<END>
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员



