
小分子药物一直是制药行业的中流砥柱。药融咨询梳理出的2024年全球十大重磅小分子药物,涵盖了多个治疗领域,从血液瘤到罕见心肌病,再到乳腺癌等,不仅展示了小分子药物在医药市场中的重要地位,也预示着未来治疗的发展方向。
本文基于药融咨询发布的《2024年十大重磅小分子药物》报告部分内容,深入剖析了其中五款极具影响力的药物——Imetelstat、Acoramidis、Capivasertib、Pirtobrutinib及Ensifentrine。通过详尽分析,揭示这些药物所蕴含的创新价值,探讨它们在未来市场中的巨大潜力,为患者带来前所未有的治疗希望与生命质量的显著提升。
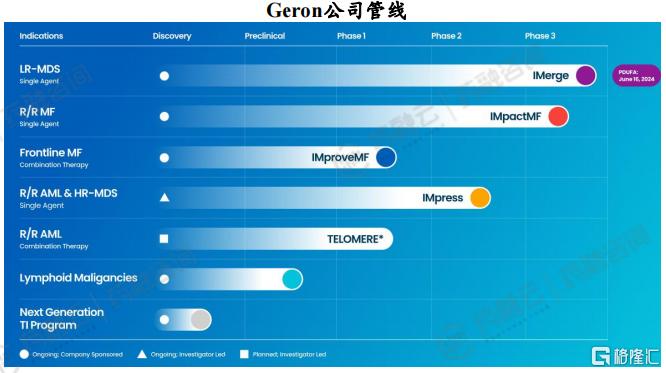
一、Imetelstat(Geron):血液瘤治疗新突破
1. 针对血液瘤,全球首款重磅端粒药物
Imetelstat是Geron公司开发的一种具有脂质片段的13-mer寡核苷酸,可特异性结合人类端粒酶的RNA模板,作为一种有效的、竞争性的端粒酶活性抑制剂,Imetelstat是首款在FDA申报上市的端粒酶抑制剂,用于治疗低危骨髓增生异常综合征(LR-MDS)患者的输血依赖性贫血。
端粒/端粒酶:端粒是存在于真核细胞线状染色体末端的一小段DNA-蛋白质复合体,端粒重复序列与端粒结合蛋白一起构成了特殊的“帽子”结构,其作用是保持染色体的完整性和控制细胞分裂周期;端粒酶由RNA和蛋白质组成,可维持端粒长度,端粒酶在85%~90%的恶性肿瘤细胞中表达上调,使得这些细胞持续且不受控制地增殖,驱动肿瘤的生长和发展,端粒酶被认为是肿瘤治疗中的一个有潜力的分子靶点。
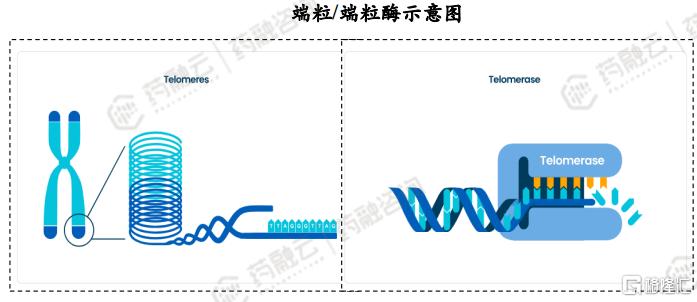
2. MDS患者尚存在未满足临床需求,新型药物亟待开发
骨髓增生异常综合征(MDS)是一组起源于造血干细胞的肿瘤性疾病,主要特征是骨髓造血功能异常、血细胞发育异常,表现为难治性的血细胞减少、造血功能衰竭,流行病学数据显示,MDS发病率约10-12/10万人口,多累及中老年人,50岁以上的病例占50%~70%,男女之比为2:1,约30%-60% MDS患者转化为白血病。
去甲基化药物阿扎胞苷、地西他滨和造血干细胞移植是骨髓增生异常综合征患者治疗的主要方式;与大多数血液恶性肿瘤相比,MDS 的批准治疗方案仍然较少,尚需应用更精准的药物来改善患者的治疗结果。

3. III期临床试验结果积极,销售峰值有望达20亿美元
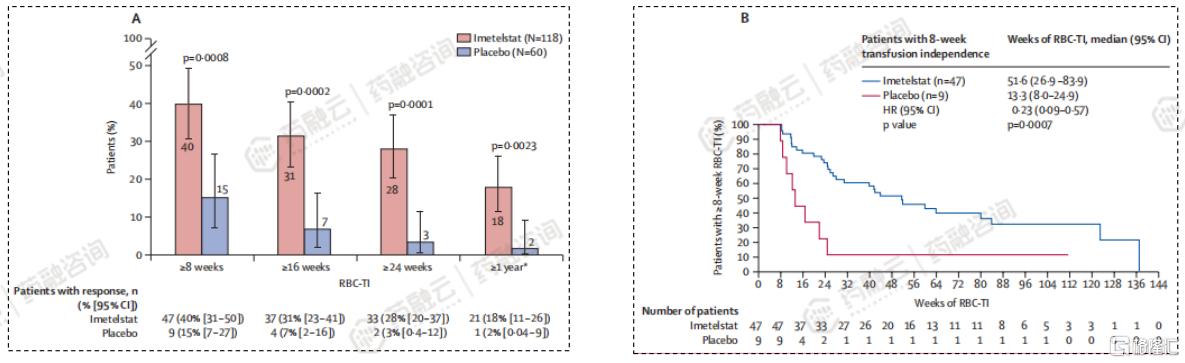
主要终点为8周RBC输注独立性(TI)率。Imetelstat组(n=118)治疗8周时TI率为39.8%,而安慰剂组(n=60)为15.0%。
关键次要终点包括24周的RBC-TI率、TI持续时间和红系反应(HI-E)等。Imetelstat组和安慰剂组的24周TI率分别为28.0%和3.3%;在Imetelstat组中,47例(40%)患者RBC-TI至少为8周,安慰剂组为9例(15%)。
安全性方面,Imetelstat组和安慰剂组3-4级治疗期间出现AE的发生率分别为91%(107/118)和47%(28/59),接受Imetelstat治疗的患者中,最常见的3-4级治疗期间出现的AE是中性粒细胞减少,Imetelstat组80例(68%),安慰剂组2例(3%),以及血小板减少,Imetelstat组73例(62%),安慰剂组5例(8%),没有与治疗相关的死亡报告。
Imetelstat 具有成为重磅炸弹的潜力,有Stifel分析师估计,Imetelstat的年销售额峰值或可达 20 亿美元。
二、Acoramidis(BridgeBio):罕见心肌病治疗新希望
1. 转甲状腺素蛋白(TTR)稳定剂,治疗罕见心肌病
Acoramidis是BridgeBio公司开发的一种口服、强效、高选择性小分子转甲状腺素蛋白(TTR)稳定剂,旨在模拟具有保护作用的转甲状腺素蛋白(TTR)T119M突变的功能,维持TTR蛋白的正常四聚体构象,从而阻止具有毒性的淀粉样蛋白的产生,用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)。
ATTR-CM是一种罕见的心肌病,主要是由于TTR基因突变,引起TTR蛋白异常解聚形成异常物质(淀粉样物质)沉积于心脏,表现为限制性心肌病和进行性心力衰竭,根据有无TTR基因突变可以将该疾病分为遗传型/突变型(hATTR)和野生型(ATTRwt)。一项系统研究结果显示,ATTR-CM的患病率估计为5.2例/百万人,发病率约为0.3例/百万人/年。
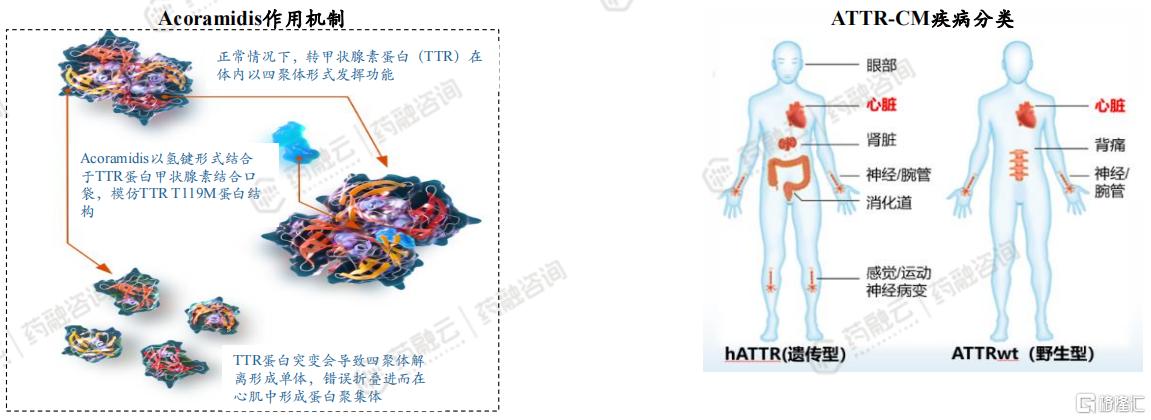
2. Acoramidis为第二款治疗ATTR-CM的TTR稳定剂
据药融云数据库统计,治疗转甲状腺素蛋白淀粉样变心肌病的已上市药物有1款,为辉瑞的Tafamidis, Tafamidis也是首个已被证实对治疗ATTR-CM有效的TTR 稳定剂。
Acoramidis是第二款在研TTR稳定剂,美国FDA已接受Acoramidis用于治疗ATTR-CM的新药申请,预定PDUFA日期为将2024年11月29日;上市后,Acoramidis将成为全球第二款治疗ATTR-CM的药物,将与辉瑞直接竞争市场份额。此外,还有多家大药企入局ATTR-CM赛道,比如再生元、诺和诺德、Ionis等。
ATTR-CM药物竞争格局
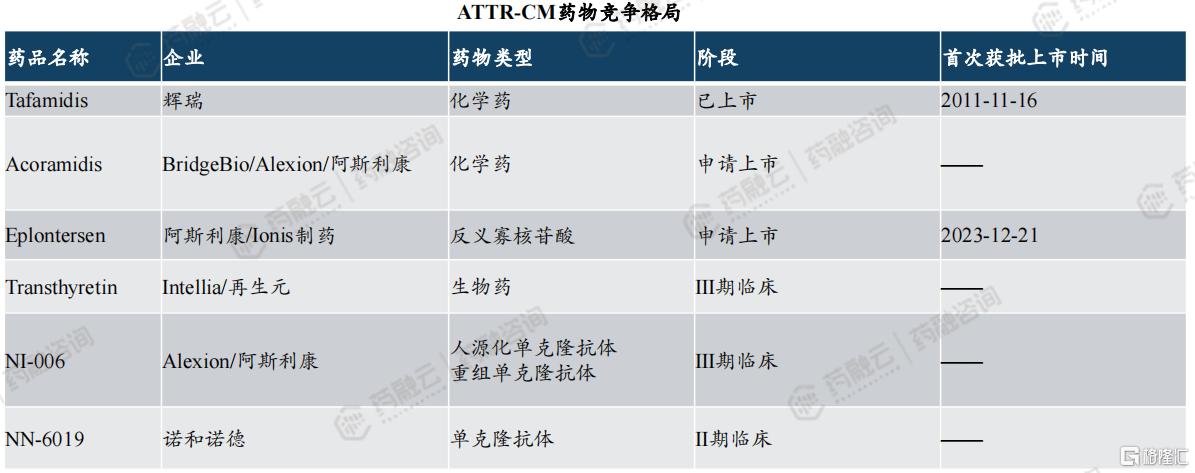
图片来源:药融咨询《2024年十大重磅小分子药物》
3. Tafamidis 2023年销售高达33.21亿美元,Acoramidis销售有望达18亿美元
辉瑞Tafamidis于2019年5月获FDA批准上市,2023年Tafamidis系列药物全球销售额高达33.21亿美元,是辉瑞全年销售额TOP10的药物,2021-2023年Tafamidis全球销售额分别为20.15、24.47、33.21亿美元。
Acoramidis为第二款治疗ATTR-CM的TTR稳定剂,Leerink Partners分析师认为,至2030年,该药的销售额可能达到18亿美元。
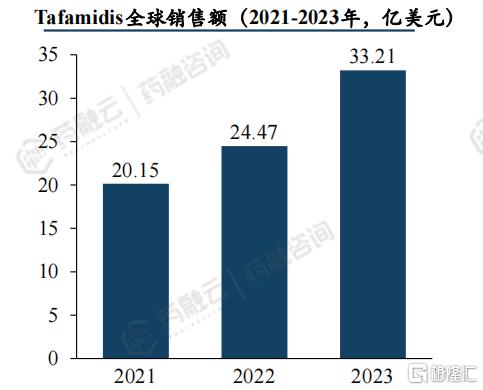
从辉瑞的Tafamidis销售业绩来看,ATTR-CM是一个重磅炸弹辈出的赛道,未来竞争格局如何,市场很快将给出答案。
三、Capivasertib(阿斯利康):HR阳性乳腺癌患者新选择
1. 全球首款AKT抑制剂,治疗HR+/HER2-晚期乳腺癌
Capivasertib是一款口服全身性pan-AKT抑制剂,由阿斯利康开发用于治疗包括乳腺癌、前列腺癌在内的多种癌症,Capivasertib于2023年11月在美国获得首次批准,联合氟维司群用于治疗激素受体 (HR) 阳性、人表皮生长因子受体 2 (HER2) 阴性、局部晚期或转移性乳腺癌的成年患者,是全球首个获批的AKT通路抑制剂。
AKT抑制剂作用机制:PAM信号通路即磷脂酰肌醇3-激酶(PI3K)-蛋白激酶B(AKT)-哺乳动物雷帕霉素靶蛋白(mTOR),该信号通路在多种肿瘤中异常激活,参与调控肿瘤细胞增殖、分化和凋亡等,是抗肿瘤药物研发所关注的重要通路;AKT位于 PI3K-AKT-mTOR 通路的核心位置,具有 3 种亚型,AKT1、AKT2 和 AKT3,三者具有高度相似的结构;超过50%的肿瘤中AKT过度活化,尤其在复发性卵巢癌、乳腺癌和前列腺癌等瘤种中更为普遍,对AKT进行抑制是肿瘤靶向药物开发的方向之一。

2. 临床Ⅲ期研究取得突破性结果,PFS和OS均显著获益
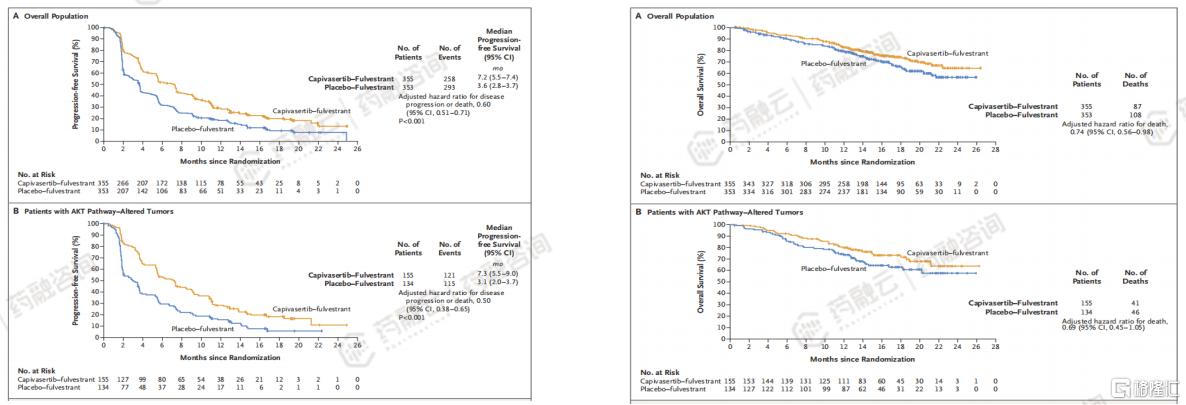
Capivasertib+氟维司群组vs安慰剂+氟维司群组,在伴有或者不伴有AKT通路异常的患者人群的中位PFS获益均表现出显著优势。在总人群中:7.2个月vs3.6个月,HR=0.60;95% CI 0.51–0.71;p<0.001;在AKT通路异常人群中:7.3个月vs3.1个月,HR=0.50;95% CI 0.38–0.65;p<0.001;在不伴有AKT通路异常人群中:7.2个月vs3.7个月,HR=0.70;95% CI 0.56–0.88;p<0.001。
Capivasertib+氟维司群组vs安慰剂+氟维司群组能更大程度降低疾病死亡风险,在伴有或者不伴有AKT通路异常的患者人群均有一致OS获益。在总人群中,Capivasertib+氟维司群组18个月的OS率为73.9%,而安慰剂组为65.0%(HR=0.74;95% CI 0.56-0.98);在AKT通路异常患者中,两组18个月的OS率分别为73.2%和62.9%(HR=0.69;95% CI 0.45-1.05)。
3.全球多款AKT抑制剂进入临床,Capivasertib销售额至少为10亿美元
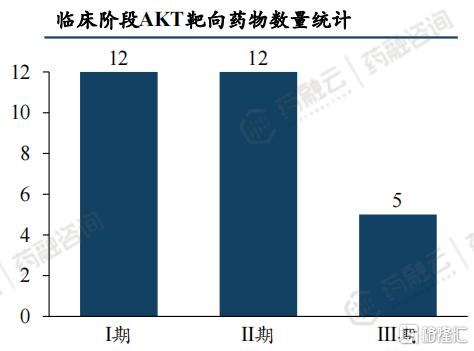
据药融云数据库统计,全球已上市AKT靶向药物仅1款,即阿斯利康的Capivasertib;在研管线中有29款产品进入临床研究阶段,其中,临床Ⅲ期5款,临床Ⅱ期12款,临床Ⅰ期12款,涉及默克、GSK、罗氏、来凯医药、先声药业等企业。
据Clarivate预测,Capivasertib到2031年将在G7(七国集团,加拿大、法国、德国、意大利、日本、英国和美国)市场获得至少10亿美元的销售额。
AKT抑制剂竞争格局
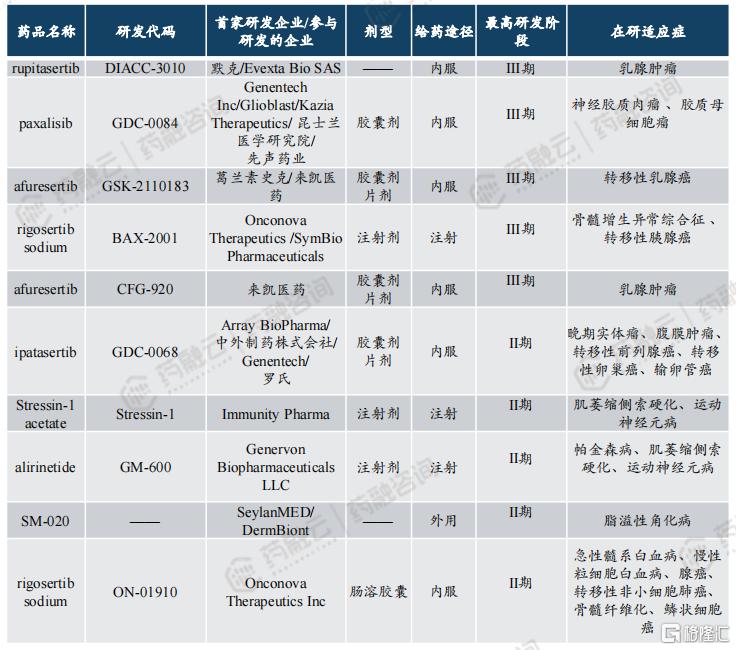
图片来源:药融咨询《2024年十大重磅小分子药物》
四、Pirtobrutinib(礼来):BTK抑制剂耐药新治疗方案
1. 首个BTK非共价抑制剂,有望解决耐药问题
Pirtobrutinib(Jaypirca)是礼来开发的一款非共价、具高度选择性的BTK抑制剂,是获FDA批准的首个非共价(可逆转)BTK抑制剂,同时也是首个获批用以治疗已对BTK共价抑制剂产生抗性的MCL患者的BTK抑制剂。
Pirtobrutinib有望解决耐药问题。第一代、第二代BTK共价抑制剂在作用方式上均通过不可逆地与BTK激酶结构域中的C481残基结合发挥作用,若患者产生BTK耐药突变,会使此类药物不能与C481残基结合,产生脱靶效应,患者治疗过程可能会中断;与前两代BTK共价抑制剂不同,Pirtobrutinib与C481没有直接的相互作用,对BTK的选择性更高,可减少治疗产生的不良事件,可能解决前两代BTK抑制剂耐药问题,为患者带来全新的治疗方案。
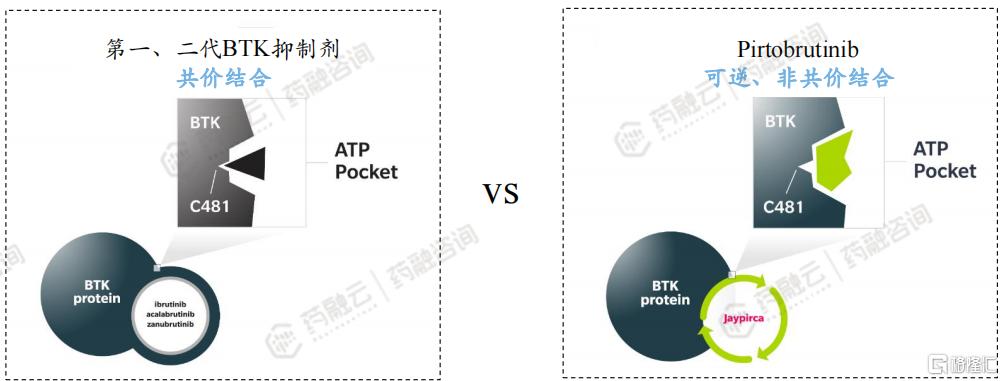
2. 临床数据优异,一年内获FDA两次加速批准
在Ⅰ/Ⅱ期临床试验中,Pirtobrutinib在对BTK共价抑制剂耐药的不同患者亚群中均展现出了出色的疗效和安全性,一年内获得FDA的两次加速批准,分别针对MCL和CLL/SLL患者。
在MCL患者中,接Pirtobrutinib治疗患者的总缓解率为50%,分别有13%与38%的患者达到了完全缓解和部分缓解,中位缓解时间为1.8个月(0.8-4.2),中位缓解持续时间为8.3个月,6个月DOR率为65.3%;在CLL/SLL患者中,接Pirtobrutinib治疗患者的总缓解率为72%,中位缓解持续时间为12.2个月,所有缓解均为部分缓解。
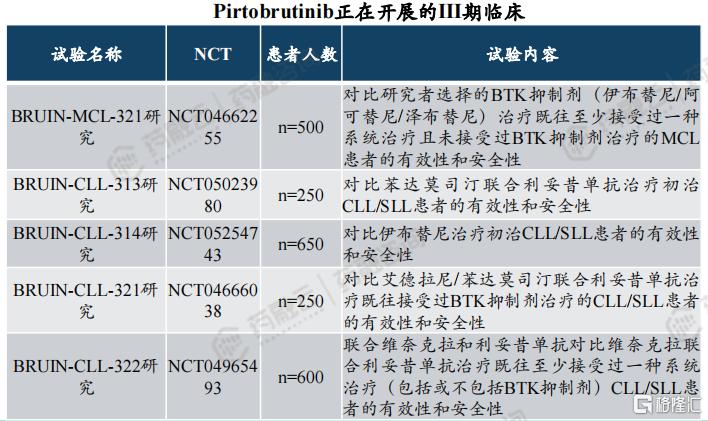
目前,礼来正在开展一项针对MCL人群的全球III期临床以及四项针对CLL/SLL人群的全球III期临床。
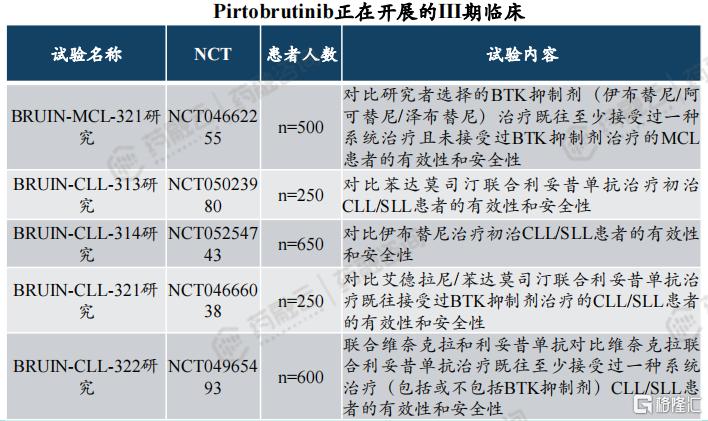
3. BTK抑制剂百亿市场规模,Pirtobrutinib销售峰值超10亿美元
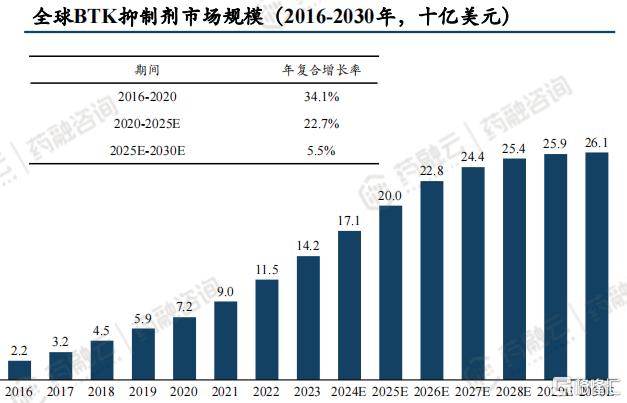
有数据显示,全球用于治疗B细胞淋巴瘤的BTK抑制剂市场规模增长迅速,从2016年的22亿美元增长到2020年的72亿美元,复合年增长率约为34.1%,预计在未来,这一市场将持续扩大,市场规模将以22.7%的复合年增长率在2025年增长至200亿美元,并持续以5.5%的复合年增长率在2030年增长至261亿美元。
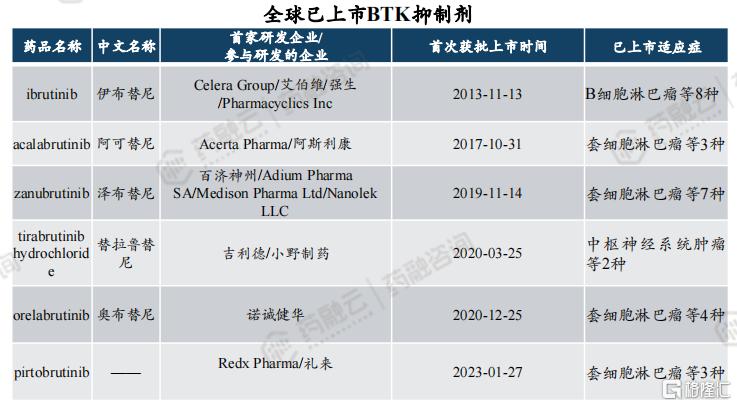
据药融云数据库统计,全球已上市BTK抑制剂总共6款,分别为强生的伊布替尼(2013年)、阿斯利康的阿可替尼(2017年)、百济神州的泽布替尼(2019年)、小野制药的替拉鲁替尼(2020年)、诺诚健华的奥布替尼(2020年)以及礼来的Pirtobrutinib(2023年)。预计Pirtobrutinib销售峰值超10亿美元。
五、Ensifentrine(Verona):慢阻肺治疗新纪元
1. PDE3/4抑制剂,慢阻肺首款新机制疗法
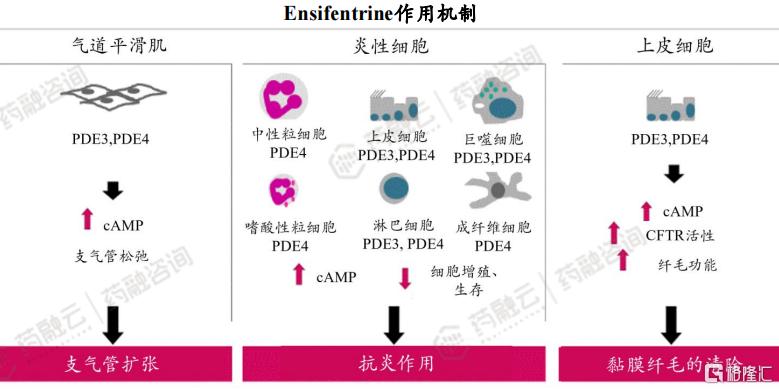
Ensifentrine是Verona研发的一款雾化吸入型磷酸二酯酶3/4(PDE3/4)抑制剂,用于慢性阻塞性肺病患者的维持治疗;Ensifentrine对PDE3和PDE4酶的双重抑制作用可产生协同效应,实现支气管扩张和抗炎效果。
2024年6月26日,FDA批准了VRNA公司的Ensifentrine(恩塞芬汀,Ohtuvayre)作为慢性阻塞性肺病(COPD)的维持治疗新药申请(NDA),标志着COPD治疗领域20多年来首次迎来了一种基于全新机制的吸入性药物。
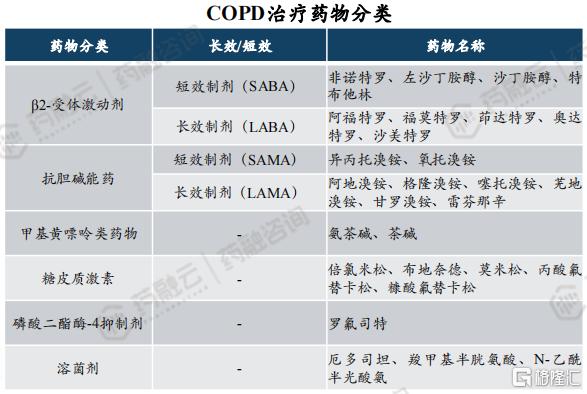
目前COPD的治疗药物主要包括β2-受体激动剂、抗胆碱能药、甲基黄嘌呤类药物、糖皮质激素、磷酸二酯酶-4抑制剂以及溶菌剂,主要用于预防和控制症状,减少急性加重的频率和严重程度,提高运动耐力和生命质量,主流起始治疗药物方案为长效β2-受体激动剂+长效抗胆碱能药。
2. Ⅲ期数据优异,优锐医药拥有大中华区权益,正在国内开展Ⅲ期临床
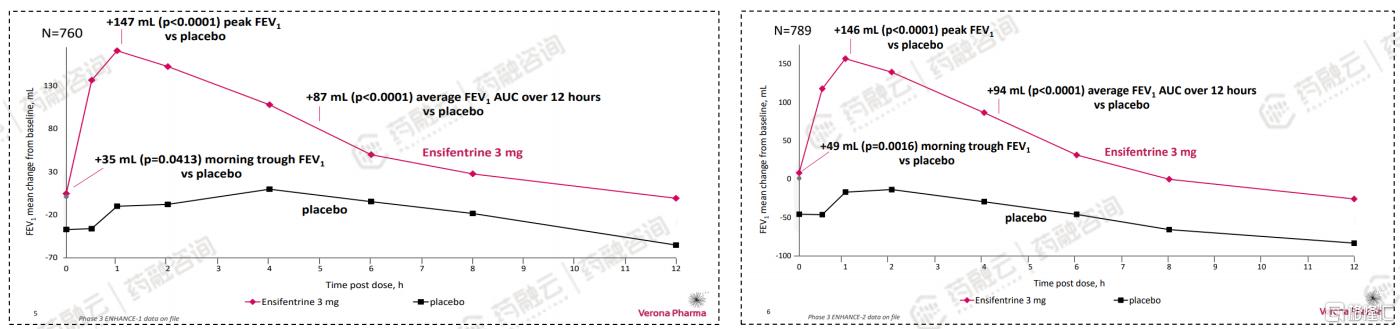
Verona在两项3期临床试验ENHANCE-1和ENHANCE-2中评估了雾化Ensifentrine作为维持疗法,治疗COPD的效果,两项试验均达到主要终点,患者肺功能获得统计显著和具有临床意义的改善;主要终点为FEV1 (一秒用力呼气容积) 0-12小时药时曲线下面积。
国内优锐医药拥有Ensifentrine大中华区权益,并于2023年2月24日启动Ensifentrine(3mg,每日2次)治疗COPD的中国III期临床试验,预计将于2025年2月完成。
3. COPD患者基数大,致死率高,市场规模超200亿美元
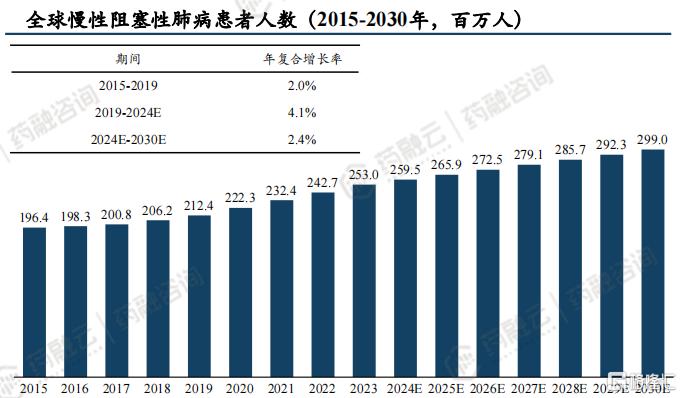
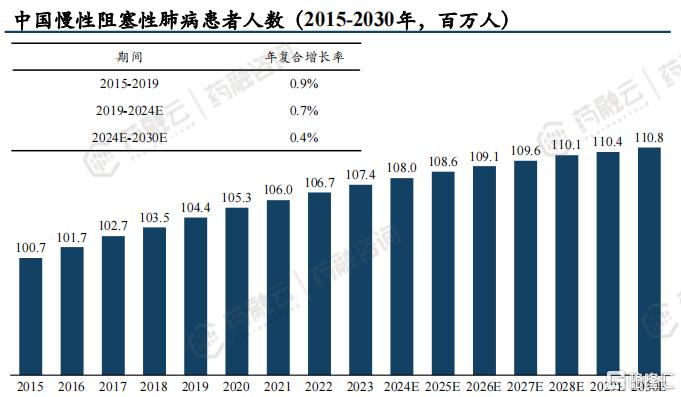
慢性阻塞性肺病是全球第三大致死疾病,仅次于脑卒中、心脏病;据测算,2024年全球COPD患者预计为2.60亿人,预计至2030年将增长至2.99亿人,2024-2030年复合增长率为2.4%;2024年我国COPD患者预计为1.08亿人,预计至2030年将增长至1.11亿人,2024-2030年复合增长率为0.4% 。
我国COPD形势亦较为严峻,每年致死人数达100万,致残人数约500-1000万,致死率及致残率均较高。
2022年,全球COPD治疗市场估计为195亿美元,预计到2030年将达到278亿美元的规模,2022-2030年复合增长率预计为4.5%。
4. PDE3/4竞争格局好,销售峰值有望超10亿美元
从竞争格局来看,数十年内无新机制COPD药物获批上市,针对PED3/4靶点,多家企业布局斑块状银屑病/特应性皮炎/COPD。同时生物制剂也积极探索COPD适应症,靶向IL-4R的度普利尤单抗率先点亮生物制剂治疗COPD的希望。
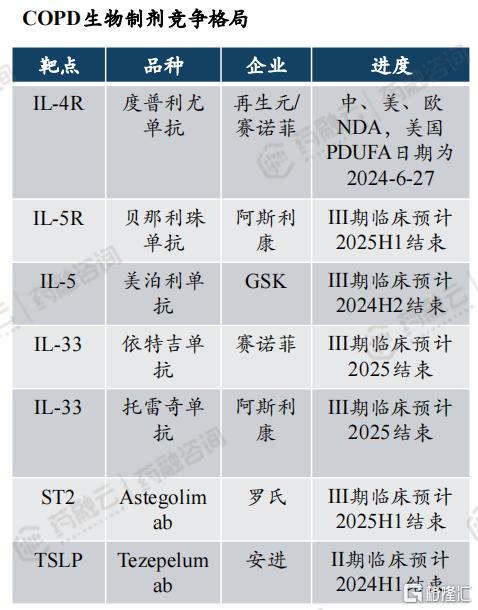
据Fierce Pharma预测,Ensifentrine 2028年销售额将达到8亿美元(上市仅4年),我们预计其销售峰值将超10亿美元。
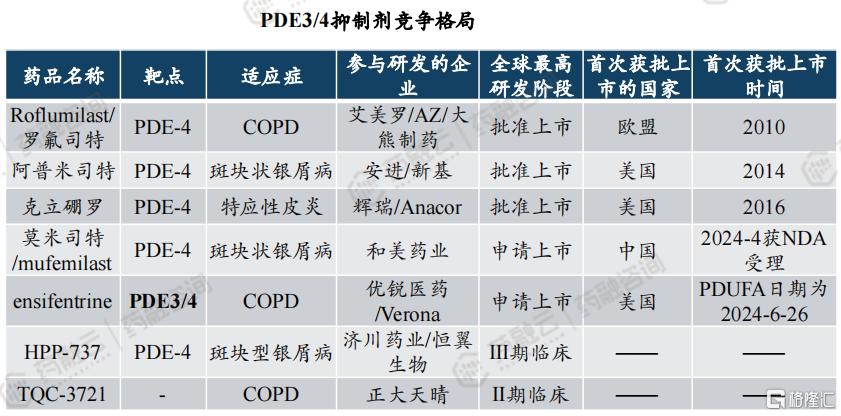
PDE4抑制剂被开发用于治疗多种炎症性疾病,包括银屑病、神经炎症、慢性阻塞性肺病(COPD)、哮喘、强直性脊柱炎(AS)、炎症性肠病(IBD)、特应性皮炎、类风湿关节炎(RA)、系统性红斑狼疮(SLE)等等。信达生物、恒瑞医药、正大天晴以及华东医药、优锐医药等国内企业都高度重视PDE4抑制剂的治疗潜力。
以上内容均来自药融咨询{2024年十大重磅小分子药物}报告,如需查看全文或下载报告,可通过浏览器前往“药融咨询”网页-资源大厅-报告大厅(https://consult.pharnexcloud.com/report)搜索报告名称获取。
<END>
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员



