4月24日,武汉波睿达生物科技有限公司(以下简称“波睿达生物”)宣布,其自主研发的CAR-T细胞治疗药物—“靶向CD99嵌合抗原受体基因修饰的自体T细胞注射液”(以下简称“BRD-03”),成功获得国家药品监督管理局(NMPA)的临床试验默示许可。
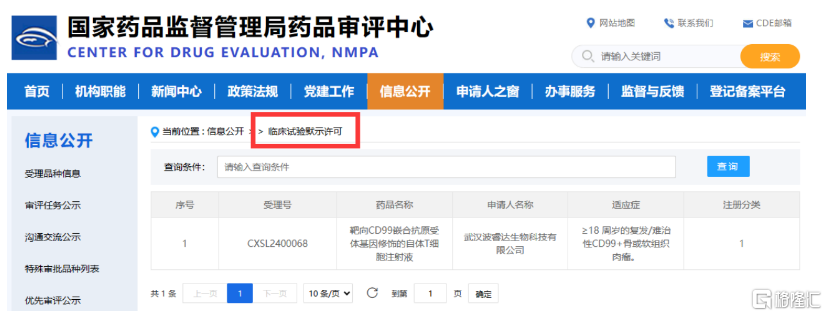
图1:BRD-03 IND获批信息(图片来源:CDE官网)
BRD-03是波睿达生物利用自主知识产权开发的全球首个靶向CD99抗原的CAR-T细胞治疗产品,主要用于治疗≥18周岁的复发/难治性CD99+骨或软组织肉瘤。
骨与软组织肿瘤是一组起源于骨或软组织等结缔组织的肿瘤,全身各部位及器官均可发病,以四肢、腹膜后或腹腔、躯干及头颈部最为常见。恶性骨肿瘤及软组织肉瘤总体发病率低,大约占成人恶性肿瘤的1%,儿童恶性肿瘤的15%。骨与软组织肿瘤的临床特点差异巨大,良性或恶性程度低者表现惰性、生长缓慢、以局部占位性生长为主;而恶性程度高者具有较强的局部侵袭性,呈浸润性或破坏性生长,且容易局部复发和远处转移,近年来虽然在研究和治疗方面有所突破,然一旦化疗失败,患者生存期一般不超过一年,临床存在迫切的需求,显示出巨大的潜在商业价值。
临床前研究显示,BRD-03对横纹肌肉瘤肿瘤细胞系等小鼠模型均有显著的抑瘤效果及较好的耐受性。BRD-03前期已开展的研究者发起的临床试验(IIT),也取得了优异的安全性与有效性的结果。
BRD-03获得临床试验默示许可,是波睿达生物在实体肿瘤免疫细胞治疗领域的重大里程碑,也必将会为CD99+骨与软组织肉瘤患者的治疗带来新的机遇和治疗选择。
CD99是由CD99基因编码的高度O-糖基化的跨膜蛋白,是一种细胞表面蛋白,高表达于骨肉瘤(osteosarcoma,OS)、尤文肉瘤(Ewing's sarcoma,ES)和横纹肌肉瘤(rhabdomyosarcoma,RMS)上。
BRD-03是由波睿达生物历时4年自主研发,拥有自主知识产权的1类治疗用生物制品。BRD-03在前期的体外研究、动物实验和探索性临床研究中,显示出极强的靶向杀瘤能力和良好的安全性。
关于波睿达生物武汉波睿达生物科技有限公司是一家致力于CAR-T免疫细胞药品研发、中试和申报于一体的制药企业,成立于2014年9月,由武汉科技大学生命科学与健康学院院长张同存教授领衔,来自国内外著名一流高校及科研机构的免疫学专家、临床医学专家、细胞生物学家联合创建的高科技创新型企业。公司形成了以血液肿瘤CAR-T为主导,病毒感染性疾病CAR-T、实体肿瘤CAR-T和通用CAR-T等多个研发项目并行推进的研发体系。波睿达已申请国家专利60余项,获专利授权20余项;血液肿瘤CAR-T针对白血病、淋巴瘤、多发性骨髓瘤已拥有CD30、CD19/22、CD99、CD20、BCMA等多个成熟靶点,已完成数百例临床试验研究。
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员