作者:天风医药郑薇团队
1. CFDA发布细胞制品重磅政策,紧跟国际前沿动向
2017年,全球免疫细胞治疗领域日新月异,研发领域不断突破,技术优化升级,加速为人类疾病带来新的治疗手段。今年2017年被称为免疫细胞治疗的元年,不仅仅是因为科研理论领域筑基逐步成熟,更多是因为医学理论正迅速的转化为实际应用。
1.1. 海外产品上市进度加速,两款CAR-T产品已获FDA批准
2017年,FDA批准CAR-T上市,提振科学界、患者、临床医生对于免疫细胞治疗领域的强大信心。8月30日,诺华的Kymriah率先获批上市,获批适应症是儿童和年轻成人急性淋巴细胞白血病(ALL),定价47.5万美元,并承诺无效退款。10月18日,Kite的Yescarta第二个获得FDA批准上市,适应症与诺华的不同,为成人复发或难治性大B细胞淋巴瘤,定价为37.3万美元。
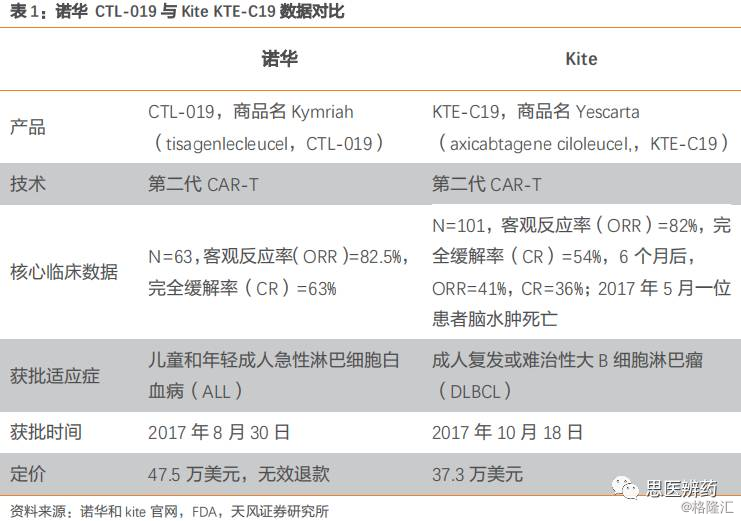
1.2. 国内政策先行,行业迎来新时代
国内加速追赶的脚步,2017年以来,陆续发布多项关于免疫细胞治疗的重磅政策,规范指导国内相关企业产品研发、注册、上市,政策红利将带来行业变革。
2016年12月,CFDA发布《细胞制品研究与评价技术指导原则》(征求意见稿),拟将免疫细胞治疗作为药品进行管理,按照药品的管理规范,包括药学研究、药理毒理研究、临床研究等阶段。
2017年12月22日,CFDA发布《细胞治疗产品研究与评价技术指导原则(试行)》,标志着我国正式开启免疫细胞治疗产品的注册上市流程,这意味着我国免疫细胞治疗产业正迎来一个全新的时代。
从此次发布的指导原则来看,将细胞治疗从医疗技术转变为药品进行统一管理,规范临床应用,并且在多个方面包括药学研究、非临床研究、临床研究等步骤进行了细化的指导,其中有三点细则建议重点关注,从这三点细则中我们认为,注册审评单位持以开放的态度与国内前沿报批企业保持密切的沟通和联系,动态调整审评审批流程,对于前期临床试验数据理想的公司,本着效率优先、支持创新、避免重复研究的原则,可以简化审批流程,缩短整体注册审批时间,兼顾安全和效率,大力鼓励创新型治疗产品快速进入市场,受益适应患者群体:
利用已有人体试验数据,或可免除动物试验
不同程度接受非注册临床试验数据,但需满足申报注册临床数据要求
以两个阶段临床试验代替传统三期临床,鼓励主动与CDE保持沟通确保方案设计合理性
1.3. 回顾我国细胞治疗行业历史,经历乱象丛生到规范化发展的过程
早期部分科室存在违规开展临床治疗,行业乱序发展。回顾政策发展历史,2009年,卫生部免疫细胞治疗技术列入第三类医疗技术,由于当时免疫细胞治疗手段的安全性、有效性尚需经规范的临床试验研究进一步验证,因此需要卫生部第三类医疗技术审核机构技术审核通过后才能开展临床试验。据新京报报道,我国批准的细胞免疫治疗的临床试验项目非常少,原国家食品药品监督管理局只批准过两个地方项目:一个是北京大学人民医院陆道培院士的CIK临床项目,还有曹雪涛院士树突状细胞(DC)项目。其他的地方医院进行的细胞免疫治疗临床试验,并没有经过批准。实际上,2015年国家第三类医疗技术应用管理政策调整之前,国家卫计委也并没有批准过任何医疗机构开展免疫细胞技术的临床应用,但是全国范围内仍然有科室违规开展免疫细胞治疗技术对患者进行治疗。
“魏则西事件”引发关注,国家强调仅限于临床研究。2016年3月,“魏则西事件”在各大媒体平台持续发酵、媒体和公众高度关注,免疫细胞治疗被推上了风头浪尖,魏则西事件使用的是DC-CIK细胞疗法,属于第三代免疫细胞疗法,不同于CAR-T。5月4日,国家卫计委医政医管局就规范医疗机构科室管理及医疗技术临床应用管理召开视频会议,紧急叫停所有违规进行细胞治疗的临床应用,并对相关要求进行了明确,已开展的项目需上报卫计委,强调免疫细胞治疗仅限于临床研究。
兼顾安全性和创新性,首个CAR-T产品进入绿色审批通道。2017年10月,中共中央办公厅、国务院办公厅印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,鼓励创新型药品、医疗器械的研发注册,加快对于具备临床应用前景、创新型、临床急需产品的审评审批速度。2017年12月11日,南京传奇生物科技有限公司提交CAR-T疗法中国临床申请(CXSL1700201)获得CDE正式承办受理,这是国内首个获得受理的CAR-T产品,同月18日,药品评审中心CDE公布第二十五批优先审评审批名单,南京传奇生物的LCAR-B38M CAR-T细胞自体回输制剂因其使用先进制剂技术、创新治疗手段、具有明显治疗优势,获准进入优先审评审批通道,加快产品审评速度。
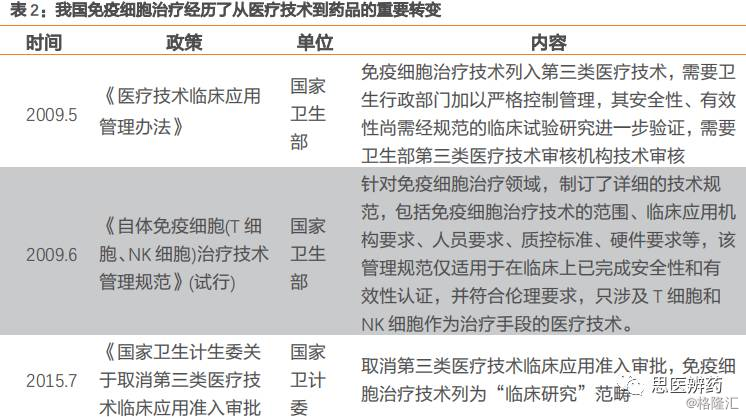

我国免疫细胞治疗产业从乱序发展到紧急叫停,后续将其作为药品进行管理,近期开始受理注册申请并且是加速审评审批状态,紧跟国际发展动态,体现出国家对于安全性的首要考量和创新型疗法的肯定,兼顾安全性和创新性,上层建筑的搭建将为产业发展开通绿色快速通道,成为我国免疫细胞治疗产业发展的加速剂。
2. 肿瘤免疫疗法再获突破,诞生划时代产品CAR-T
肿瘤免疫疗法是当前研发热点之一,CAR-T是一项具有划时代意义的突破技术。2011年,美国宾夕法尼亚大学Carl H. June 教授团队的 CAR-T 疗法在1例慢性淋巴细胞白血病(CLL)患者治疗的中获得突破,2012年,June团队使用CAR-T治疗急性淋巴细胞性白血病(ALL)7岁患者Emily,经历连续高烧后,达到完全缓解,今年12岁,已健康生活了5年。
CAR-T全名是嵌合抗原受体T细胞(Chimeric Antigen Receptor T-Cell),属于肿瘤免疫疗法大类-细胞治疗子类中最新一代的治疗技术,目前CAR-T已发展至第四代结构,但是第二代CAR-T结构的临床数据较为理想,FDA批准的诺华和Kite使用的均为第二代结构。以下将以“肿瘤免疫治疗大类-免疫细胞治疗子类-CAR-T”的顺序进行详细介绍。
2.1. 肿瘤免疫治疗优势明显,渐成抗癌新星
攻克癌症一直是人类永恒的课题,人类对癌症的治疗方法从手术治疗、放射线治疗、化学治疗,发展到较为先进的靶向药物治疗,取得了一系列长足进步,然而这些治疗方法仍然存在不同程度的局限性,相比而言,免疫治疗作为新兴的治疗方式,具备治疗效果明显、毒副作用小、作用范围广泛,通过调动机体自身的免疫力量达到抗肿瘤作用,可以持久响应等优势。

 免疫治疗广义上指的是应用免疫学的原理,人为提高肿瘤细胞的免疫原性和免疫细胞的敏感性,激发和增强机体对肿瘤细胞的免疫应答,通过免疫细胞杀伤肿瘤细胞,抑制肿瘤的生长。免疫治疗是近年来逐渐兴起的一种治疗方法,由于其治疗效果明显、毒副作用小、作用范围广泛,通过调动机体自身的免疫力量达到抗肿瘤作用,可以持久响应。近年来免疫疗法发展迅速,正逐渐成为未来肿瘤治疗的发展方向,被认为是最有可能治愈癌症的方法。目前肿瘤免疫治疗多数被应用于晚期或难以手术的肿瘤患者,但在将来有望成为癌症治疗的一线疗法。
免疫治疗广义上指的是应用免疫学的原理,人为提高肿瘤细胞的免疫原性和免疫细胞的敏感性,激发和增强机体对肿瘤细胞的免疫应答,通过免疫细胞杀伤肿瘤细胞,抑制肿瘤的生长。免疫治疗是近年来逐渐兴起的一种治疗方法,由于其治疗效果明显、毒副作用小、作用范围广泛,通过调动机体自身的免疫力量达到抗肿瘤作用,可以持久响应。近年来免疫疗法发展迅速,正逐渐成为未来肿瘤治疗的发展方向,被认为是最有可能治愈癌症的方法。目前肿瘤免疫治疗多数被应用于晚期或难以手术的肿瘤患者,但在将来有望成为癌症治疗的一线疗法。免疫治疗根据机制不同分为4类,分别为非特异性免疫刺激剂、癌症疫苗、免疫检查点阻断剂、免疫细胞疗法(免疫过继疗法)。
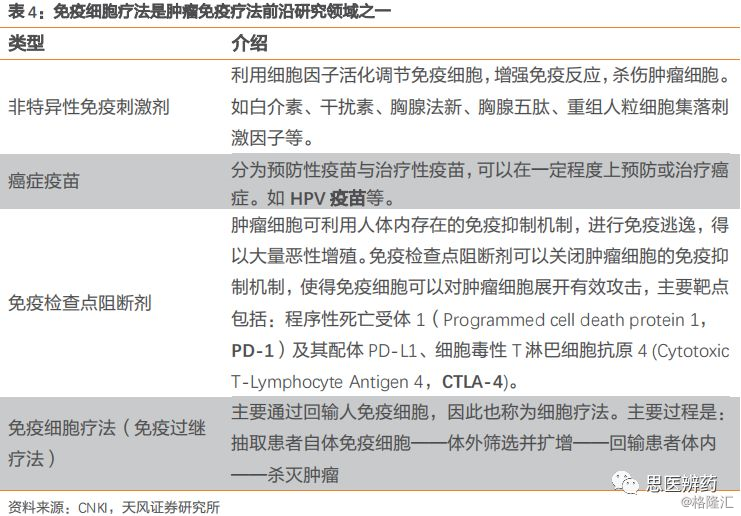
免疫细胞疗法是肿瘤免疫疗法前沿研究领域之一,也是最为火热的方向,各国研发团队积极投入,期望能在新疗法广泛应用前实现卡位布局。
2.2. 免疫细胞疗法经历从“广谱”到“精准”
免疫细胞疗法,主要通过回输人免疫细胞,因此也称为免疫细胞疗法,抽取患者自体免疫细胞,在体外进行修饰并扩增后,再回输到体内,使免疫细胞选择性的杀伤肿瘤细胞。
早期免疫细胞治疗方式,通过外界手段增强免疫细胞活性,已达到杀伤肿瘤细胞的目的,常见的治疗方式包括LAK(淋巴因子激活的杀伤细胞)、CIK(细胞因子诱导的杀伤细胞)。
第三代的DC-CIK疗法是在原有CIK细胞上增加输入了DC细胞,使其对肿瘤细胞的定向能力更强,DC细胞与CIK细胞的有机结合可产生特异性免疫和非特异性免疫的双重抗肿瘤作用。我国在DC-CIK疗法研究深入,成功发表多篇高质量文章,但其临床效应仍需要更多的实验数据支撑,魏则西事件使用的便是这种DC-CIK细胞疗法。

第四代免疫细胞疗法指的是TCR-T和CAR-T,相比于前三代,第四代涉及T细胞的转基因改造过程,理论上将更为精准更为高效的杀伤肿瘤细胞,多项临床数据显示其在血液肿瘤上的巨大潜力,FDA已经批准两款CAR-T产品上市,未来有望继续扩大临床适应症。
2.3. CAR-T,是细胞治疗更是“活的靶向创新药”
CAR-T细胞,全称是嵌合抗原受体T细胞(Chimeric Antigen Receptor T-Cell),指通过基因工程技术,将CAR(嵌合抗原受体)转到患者T细胞中,使其能够识别肿瘤特异性抗原的受体,从而达到抑制肿瘤生长、杀伤肿瘤细胞的目的。
2.3.1. CAR-T升级优化,杀伤能力更强,持续时间更久
CAR-T的结构包括胞外和胞内两部分,这些区域的不同设计都会对CAR-T效果产生影响:
1. 胞外部分主要是识别肿瘤相关抗原(如CD19)的单链抗体(抗体单链可变区,scFv);
2. 铰链区:可以促进抗原受体与肿瘤抗原的结合
3. 跨膜区:用来固定CAR
4. 胞内活性区包括T细胞活化区(提供T细胞活化的第一信号,激活T细胞的增值信号通路)和共刺激区(提供T细胞活化的第二信号,维持T细胞的生存时间)
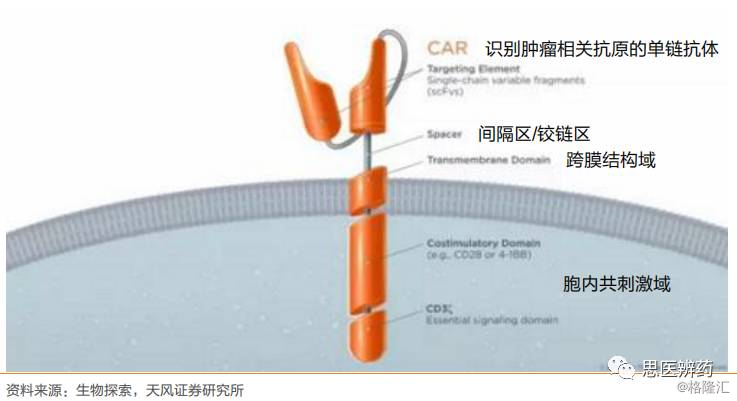 历经十余年,CAR-T经历了四代结构,每一代结构都是在各个细节上突破,最终CAR-T往更为精准、更为高效、更为持久的方向发展:
历经十余年,CAR-T经历了四代结构,每一代结构都是在各个细节上突破,最终CAR-T往更为精准、更为高效、更为持久的方向发展:
第一代CAR-T只有一个胞内信号组分,主要是CD3ζ或FcRγ,T细胞可以被活化但无法大量增殖,主要靶向不同恶性肿瘤细胞表面的L1CAM、CD20 和CAIX。其疗效一般,持久性很差,T细胞增殖减少最终导致凋亡,T细胞的抗肿瘤活性在体内受到了很大限制。
第二代CAR-T具有两个胞内信号组分,包括一个共刺激分子,如CD28、41BB、OX40 或者ICOS 和CD3ζ,这样的结构决定了T 细胞即便没有外源性共刺激分子也可以不断增殖,而且共刺激分子可以活化相关的信号通路如ERK p38、JNK 和NF-κB等。
第三代CAR-T具有三个胞内信号区,包括CD28、CD3ζ、41BB 或OX40。研究表明,胞内有三个共刺激信号的三代CAR结构使细胞具有更强的肿瘤裂解能力和更多的因子分泌,并在小鼠体内具有更强的肿瘤抑制能力。
第四代CAR-T结构与前三代不同,因表达特定的细胞因子( 目前主要是IL-12 ) 而被称为“卡车”T细胞TRUCK ( T-cells redirected for universal cytokine killing ) ,可以在具有免疫抑制性的肿瘤微环境中释放促炎性因子,从而有助于招募并活化更多的外部免疫细胞而增强免疫反应。
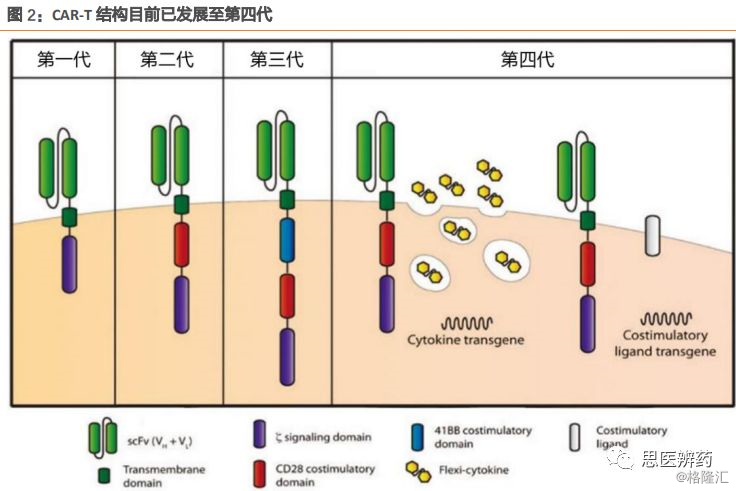 目前第二代CAR-T结构的临床数据较为理想,FDA批准的诺华和Kite使用的均为第二代结构。CAR-T结构的不断更新迭代,伴随着是修饰T细胞在体内的增值活性和存活时间,通过优化CAR-T结构,其杀伤能力更强,持续时间更久,对于患者的临床效果更为显著。
目前第二代CAR-T结构的临床数据较为理想,FDA批准的诺华和Kite使用的均为第二代结构。CAR-T结构的不断更新迭代,伴随着是修饰T细胞在体内的增值活性和存活时间,通过优化CAR-T结构,其杀伤能力更强,持续时间更久,对于患者的临床效果更为显著。
2.3.2. 细胞治疗步骤为T细胞收集-转染-过继转移-病人监测
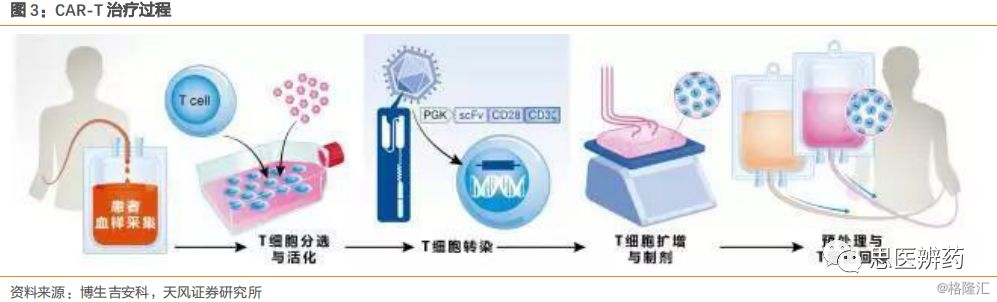
CAR-T细胞治疗具体来看主要分为4个步骤:
1. T细胞的收集:从癌症患者体内分离出免疫T细胞;
2. T细胞的转染:利用基因工程技术将能够特异性识别肿瘤细胞的CAR结构通过慢病毒、逆转录病毒、质粒等载体转染进入T细胞;
3. T细胞的过继转移:体外培养,大量扩增CAR-T细胞,一般一个病人需要几十亿乃至上百亿个CAR-T细胞(体型越大,需要细胞越多),然后把扩增好的CAR-T细胞回输到病人体内;
4. 病人的监测:严密监护病人,尤其是控制前几天身体可能的不良反应,监测响应情况和响应的持续性
 2.3.3. 相比于传统肿瘤治疗方式优势明显
2.3.3. 相比于传统肿瘤治疗方式优势明显
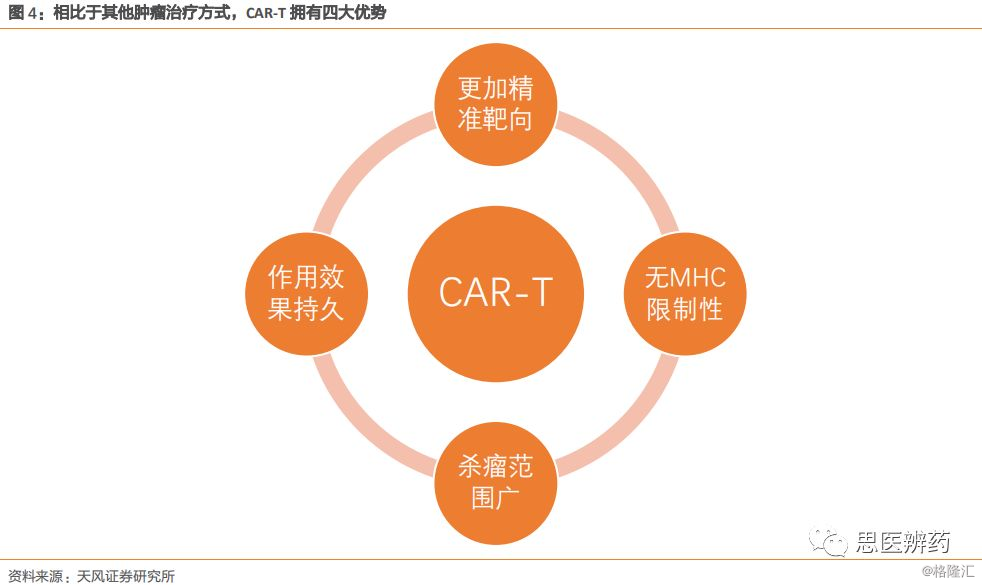
相比于其他肿瘤治疗方式,CAR-T细胞治疗作为新型的治疗手段,在诸多方面拥有优势:
1. 更加精准靶向,治疗效果极佳
CAR-T细胞治疗采用免疫的原理具有多种传统药物不具备的优点,相较于化疗药物和靶向药物,其应用基因工程修饰的病人自体T细胞,通过抗原抗体的良好结合(这种结合常比药物和靶标的结合还要好),CAR-T 的靶向性更强,在一些血液瘤中取得了良好的完全缓解率和客观响应率。
2. 作用效果更加持久
新一代CAR结构中加入了促进T细胞增殖与活化的基因序列,能保证T细胞在进入人体后还可以增殖,使得CAR-T细胞具有了免疫记忆功能,可以相当长时间在体内存活,可以持久攻击癌细胞。
3. 多靶向,杀瘤范围广
CAR可以通过技术修饰达到多靶向的目的,既可以利用肿瘤蛋白质抗原,又可利用糖脂类非蛋白质抗原,扩大了肿瘤抗原靶点范围。而且鉴于很多肿瘤细胞表达相同的肿瘤抗原,针对某一种肿瘤抗原的CAR基因构建一旦完成,便可以被广泛利用
4. 无MHC限制性
相比于同一代的TCR-T细胞治疗,CAR-T不需要识别MHC分子(主要组织相容性复合物)。由于CAR-T克服了MHC的限制性,可更有效的杀伤抗原特异性的肿瘤细胞,减少了由于肿瘤降低MHC分子表达而造成的免疫逃逸,同时打破了病人对于MHC的限制后,CAR改造的T细胞相对于天然T细胞表面受体TCR能识别更广泛的目标。
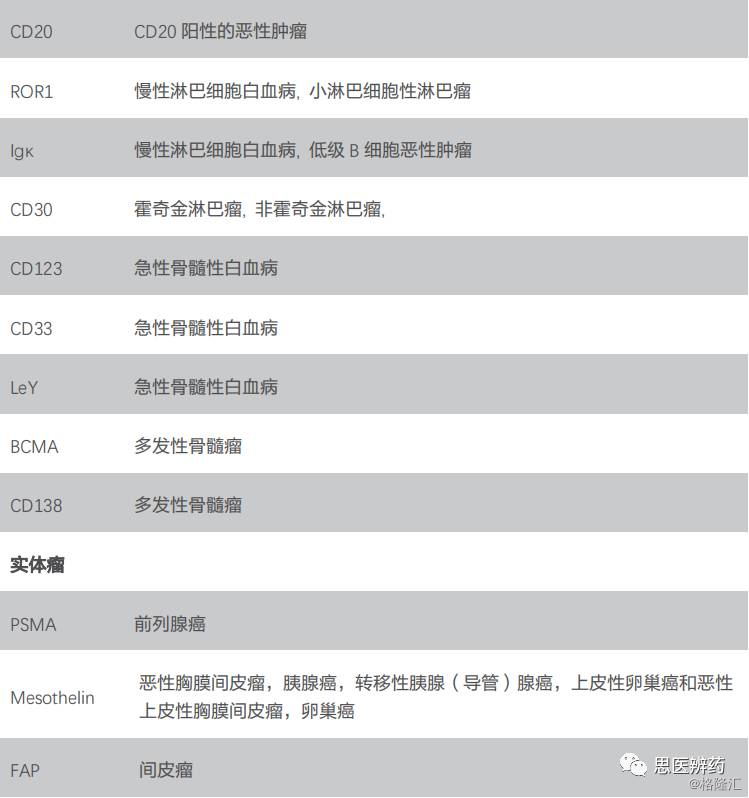
2.3.4. CAR-T目前主要应用于血液肿瘤,未来有望向实体瘤突破
CAR-T细胞可以特异性地识别肿瘤相关抗原,使效应T细胞的靶向性、杀伤活性和持久性较常规应用的免疫细胞大幅提高。目前,CAR-T细胞免疫疗法在白血病、淋巴瘤、黑色素瘤、脑胶质瘤等恶性肿瘤治疗中均显示出良好的抗肿瘤效应。随着这个研究热门领域相关技术的快速进步,未来也可能会克服肿瘤局部免疫抑制微环境,从而打破宿主免疫耐受状态,杀灭实体肿瘤细胞。
在血液肿瘤方向,CD19无疑是竞争最为激烈的靶点,随着诺华和Kite产品获得FDA批准上市,CD19的有效性被进一步肯定。此外,CD22、CD20、CD30等位点同样也是研究热点。除了目前研究较为深入的血液肿瘤领域,已有不少研究团队将CAR-T瞄准具有更大市场空间的实体瘤领域,实体瘤的研究热门靶点包括Mesothelin、GD2、HER2等。


CD19靶点对应的适应症率先获得FDA批准上市,从诺华KTE-C19的临床试验数据来看,CAR-T疗法对于儿童以及患有复发性或难治的急性淋巴性白血病的成人而言,客观缓解率高达80%-90%;非霍奇金淋巴瘤(NHL)患者在接受CAR-T疗法(Kite CTL-019)治疗后,82%的患者症状得到了缓解,完全缓解率达到54%。
仅从完全缓解率分析,传统的药物化疗已经可以达到8成左右的完全缓解率,目前CAR-T在临床试验中的结果缓解率相比较低。但是药物化疗具有很大复发的可能性,而且具有较大的毒副作用,CAR-T产品则在这方面变现由于药物化疗。
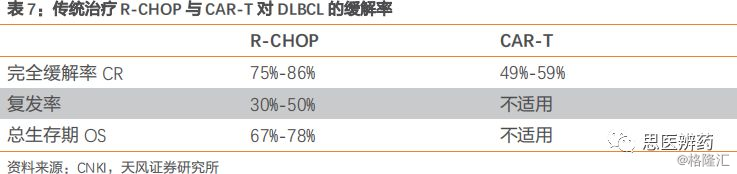
未来随着CAR-T渗透率提升、适应症扩大、价格逐步下降,市场空间有望继续扩大,近期已有不少研究机构开始CAR-T的实体瘤研究,并且有些获得了理想的数据,实体瘤的市场规模远大于血液肿瘤,未来行业空间有望持续扩大。
3. 全球CAR-T市场指数级增长,国内存量市场空间或达285亿人民币
Coherent Market Insights预计,2017年全球CAR-T细胞治疗市场估值为7200万美元,2028年将达到85亿美元,2019年至2028年间市场规模预计呈指数增长,复合年增长率高达46.1%。

目前主要应用的两类适应症为儿童和年轻成人急性淋巴细胞白血病(ALL)和非霍奇金淋巴瘤(NHL,成人复发或难治性大B细胞淋巴瘤),根据《2017年中国癌症统计》,中国因白血病每年死亡人数为4人/10万人,淋巴瘤死亡人数为3.4人/10万人,以14亿人口计算,白血病每年死亡人数为5.6万人,淋巴瘤4.76万人。其中,急性淋巴细胞白血病(ALL)约占白血病病例的25%,非霍奇金淋巴瘤(NHL)占淋巴瘤比例约为90%,对应死亡人数为1.4万人、4.3万人,合计5.7万人。参考国内肿瘤靶向治疗药物,预计CAR-T疗法市场价格约为40-50万元人民币/疗程,我们预测中国存量市场空间约为228-285亿元。
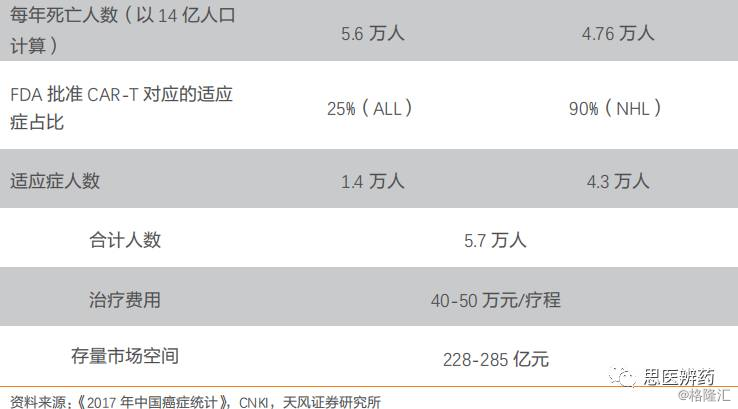
海外市场受益于政策红利、大额科研投入、技术前沿等优势,率先启动CAR-T产品上市进程,但是国内政策制定者积极响应,构建上层建筑,为CAR-T产品构建上市通道,我们认为在CAR-T领域,中国紧紧抓住时代的潮流,行业正迎来发展良机。
4. 海外CAR-T三巨头并驱争先,诺华率先获批
在CAR-T疗法的开发上,美国大幅领先,中国紧随其后,欧洲和日本明显落后。美国是CAR-T技术的起源地,诺华、Kite和Juno在CAR-T疗法在产品研发上均处于领先地位,其中两家的产品已获FDA批准上市,引领CAR-T产业的发展。另外还有多家小型生物医药公司也分别在各自领域取得了一定突破,其CAR-T产品各具特色,比如Cellectis(使用异体T细胞)、西比曼(实体瘤)等。
4.1. 诺华:稳扎稳打,Kymriah率先上市
2017年7月12日,FDA肿瘤药物专家咨询委员会在评审会议上以10:0的结果全票通过诺华的突破性CAR-T疗法的上市申请。2017年8月30日,FDA正式批准诺华CAR-T疗法 Kymriah(tisagenlecleucel,CTL-019)上市,用于治疗儿童和年轻成人(2~25岁)急性淋巴细胞白血病(ALL),比预定的时间提前了5周,成为全球首个获批的CAR-T免疫细胞疗法。在新闻公告中,FDA明确将CAR-T疗法 Kymriah划分为以细胞工程为基础的基因治疗产品,Kymriah也是FDA批准的第一个基因治疗药物,具有划时代的意义。
Kymriah疗效明显,完全缓解率达到82%。诺华的CAR-T主打产品为Kymriah,是属于第二代CAR-T疗法,2016年末的ASH会议上,诺华公布了临床2期ELIANA的数据,Kymriah针对儿童或年轻患者的复发或难治性的急性B细胞型淋巴性白血病(ALL)的完全缓解率达到82%。
不同于Juno失败案例,诺华使用更为安全的CAR-T结构。Kymriah是诺华与宾夕法尼亚大学共同合作开发的CAR-T疗法,是通过嵌合抗原受体的4-1BB共刺激域来增强细胞扩增和效力。据美国癌症研究学会(AACR)年会上公布的研究显示,相比于Juno早期使用的CD28,嵌合抗原受体上采用4-1BB刺激域的技术特点是可以使细胞体内扩增相对温和,存续时间更长,复发率也更低。
诺华旗下后续的CAR-T研发管线并不多,但是CAR-T产品的开发非常稳健,也是几大CAR-T领先企业中走在最前面的,未来有望实现业绩增量。诺华对Kymriah的定价是一个疗程47.5万美元,约300万元人民币左右,但诺华同时也承诺无效退款,来节省无效的医疗费用。
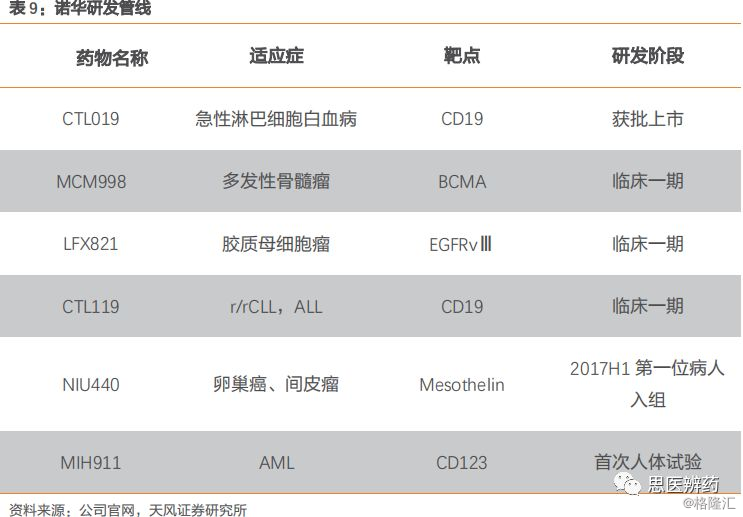
2017年10月31日,诺华宣布已经向FDA递交了CAR-T产品Kymriah的补充生物制品许可申请,寻求扩大适应症,用于治疗不适合接受自体干细胞移植的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)患者。Kymriah在4月份曾获得FDA针对该适应症授予的突破性药物资格。此外,诺华还计划在2017年底向欧洲药品管理局(EMA)提交Kymriah用于治疗急性B细胞型淋巴性白血病(ALL)和弥漫大B细胞淋巴瘤(DLBCL)的上市申请,并计划2018年向美国和欧洲之外的国家提交上市申请。
4.2. Kite Pharma:Yescarta获批上市,CAR-T管线丰富
Yescarta(axicabtagene ciloleucel,,KTE-C19)是Kite Pharma公司开发的一种靶向CD19的CAR-T疗法。2017年10月18日,FDA正式批准其用于治疗对其他疗法无响应或者接受过至少2种治疗方案后复发的特定类型成人大B细胞淋巴瘤患者,包括弥漫性大B细胞淋巴瘤、转化型滤泡性淋巴瘤、原发纵隔B细胞淋巴瘤。弥漫性大B细胞淋巴瘤(DLBCL)是成人中最常见的非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL),美国每年约有72000例NHL新病例被确诊,DLBCL占了约三分之一。
这是继诺华的CAR-T免疫疗法Kymriah之后,美国FDA批准的第二款CAR-T疗法。值得一提的是,Yescarta是首款获批用于治疗特定类型非霍奇金淋巴瘤(NHL)的基因疗法。Yescarta的安全性和有效性在一个包含100多名复发或难治性大B细胞淋巴瘤成人患者的多中心临床试验中得到了验证。此前,FDA曾授予Yescarta优先审评资格、突破性疗法认定以及孤儿药认定。Gilead /Kite对其CD19靶向疗法Yescarta的定价为37.3万美元每例患者,低于诺华Kymriah 47.5万美元的定价。
2017年7月31日,Kite制药宣布向欧洲药品管理局(EMA)提交了KTE-C19的上市申请,用于治疗不适合接受干细胞移植的复发或难治性大B细胞淋巴瘤、转化型滤泡性淋巴瘤、原发性纵隔大B细胞淋巴瘤患者。Kite也是第一家向欧盟递交CAR-T疗法上市申请的公司,并获得加速审批资格。
Kite深耕CAR-T领域,具有丰富的CAR-T产品研发管线。同时Kite Pharma全球开发进程也不断突破:与日本第一三共合作,转让了KTE-C19的日本市场权利;2017年初宣布与复星医药进行合作,成立合资公司-复星凯特生物,正式开始CAR-T细胞治疗的中国本土化进程。2017年8月28日Gilead宣布以高达119亿美元将Kite收购,Kite成为了Gilead的子公司。
Yescarta(axicabtagene ciloleucel,,KTE-C19)除了已经获批的适应症,其他适应症临床试验也在紧锣密鼓的进行着,目前已进入临床二期的适应症包括惰性非霍奇金淋巴瘤、侵袭性非霍奇金淋巴瘤、髓细胞白血病。此外,另外4款CAR-T产品的临床试验也已经逐步开展。
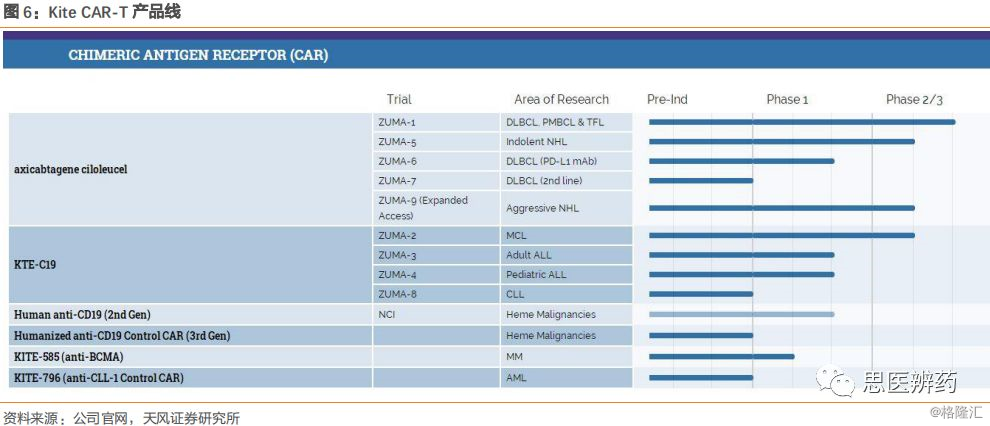
Kite同时也在积极布局TAR-T产品的临床试验研发,产品适应症以实体瘤为主,约有一半的产品进入临床一期。
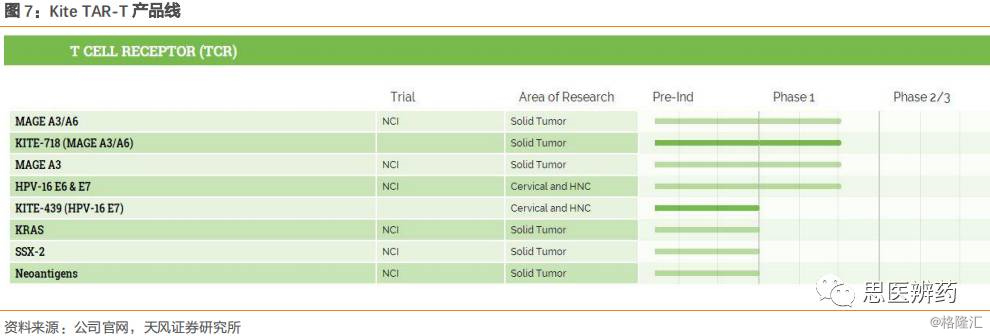
Kite CAR-T疗法的获批也与中国市场相关,2017年1月,Kite和复星医药达成战略合作,双方共同出资在中国成立了一家合资公司,旨在向中国市场引进Kite的KTE-C19(axicabtagene ciloleucel)、KITE-439 、KITE-718 等T细胞免疫治疗领域相关产品。
4.3. Juno:暂时受挫,底蕴依旧
Juno是最早一批进入CAR-T研发的公司,其前瞻性研究一直引领着行业的发展,某种程度上代表CAR-T临床应用的最新进展,吸引着众多投资者的关注。但在2016年,Juno的CAR-T候选明星产品JCAR015临床试验中的一连串死亡事件严重阻碍了CAR-T产品推出市场的日程。2017年03月,Juno正式宣布放弃JCAR015的开发,由于其他CAR-T产品仍然处于临床试验阶段,产品进程落后于其他公司,Juno跌出了首批CAR-T产品上市竞争中的第一梯队。
不同于诺华获批的Kymriah使用4-1BB共刺激分子,Juno的JCAR015使用的是CD28。2014年,在美国癌症研究学会(AACR)年会上有研究显示,CD28与4-1BB相比存在重大缺陷。CD28的特点是刺激CAR-T细胞在体内迅速扩增,但同时也使得细胞迅速耗竭,复发率较高,而4-1BB的技术特点是细胞体内扩增相对温和,但存续时间更长,复发率也更低。尽管Kite获批的KTE-C19同样使用的是CD28,但由于Kite为了避免与诺华、Juno展开直接竞争,选择了不同的适应症,将产品中心放在淋巴瘤,而淋巴瘤CAR-T治疗产生的细胞因子风暴比起急性白血病更为温和可控,才避免出现多例死亡事件,在超过100例的实验中仅出现了1例脑水肿死亡案例,对于复发难治、临床无其他治疗手段的恶性疾病患者来说,是在可接受的范围内。
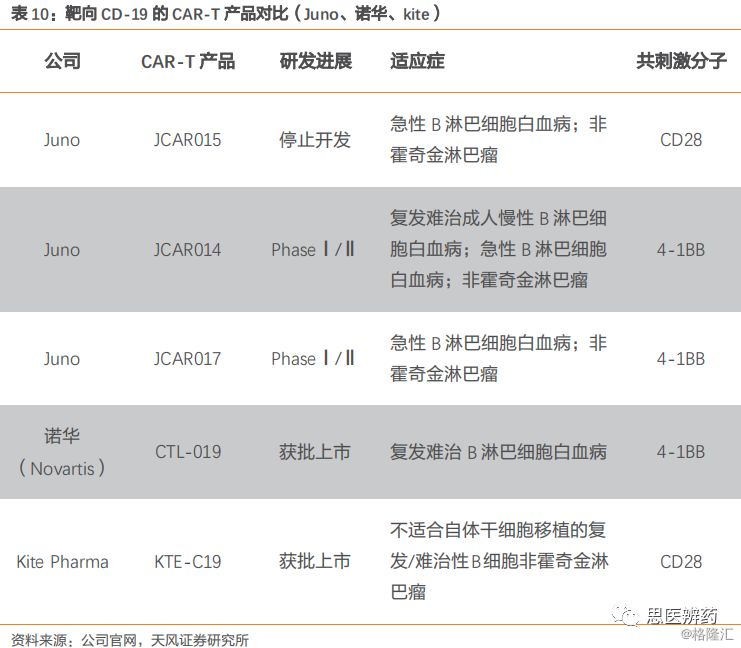
虽然JCAR015项目停止开发,但Juno的其他CAR-T产品并未受影响。作为CAR-T领域的龙头之一,Juno仅针对CD19靶标就有3款产品,另外2款产品(JCAR014和JCAR017)不同于失败产品JCAR-015,其共刺激结构域不再使用CD28,而是使用与诺华相同的4-1BB,实际上,Juno在2015年前后获得4-1BB技术,并在近年逐渐转向使用慢病毒载体的4-1BB方案。目前JCAR014和JCAR017已进入临床二期试验,有望快速赶上诺华和Kite。
尽管Juno在JCAR015受挫,但是Juno底蕴依然深厚,除了CD19靶点之外,Juno还在积极开发其他如CD22、WT1等靶点的CAR-T疗法,以开发针对不同适应症的产品。研发储备丰富,未来几年有望陆续推出CAR-T产品,深度布局免疫细胞治疗领域。

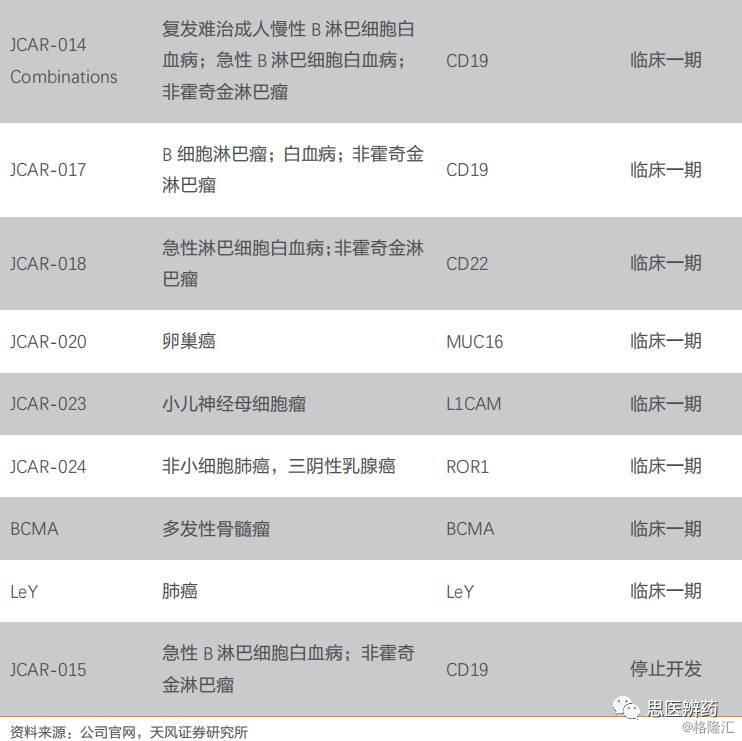
此外,Juno深耕CAR-T领域,积极开发升级版的CAR-T疗法,其中一个是双特异性的CAR-T疗法。相比于目前主流的单抗,Juno新加入的第二个特异性受体可以是激活型信号也可以是抑制性信号。以抑制性信号iCAR为例,其可以特异性识别健康组织中存在的靶标蛋白,如下图中的antigenB。在癌症组织中,CAR识别antigenA杀伤癌细胞,但是正常组织中,antigenB结合iCAR,启动抑制信号,T细胞不会杀伤带有靶标antigenA的正常细胞,从而保护了正常细胞,提高了CAR-T疗法的特异性和安全性。
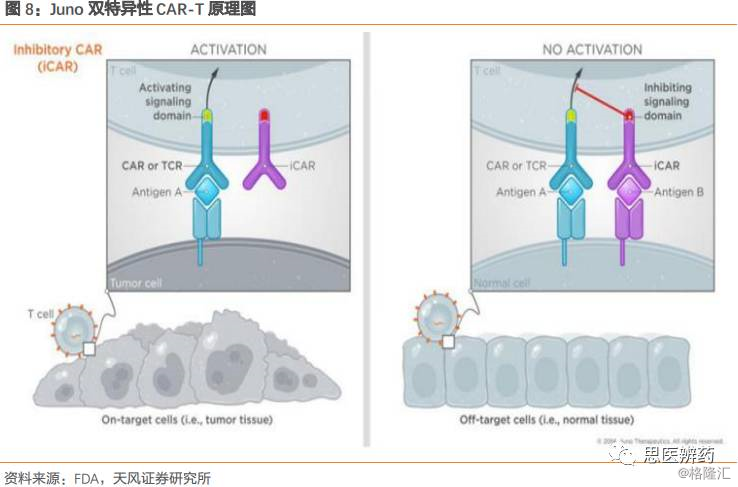
尽管深耕CAR-T多年的Juno没能获得首个产品上市,但是其研发储备丰富,在目前火热的CD19靶点上仍然有2个在研产品,并且已经进入了临床二期阶段,此外还有其他靶点的布局,我们认为未来Juno潜力巨大,后续建议密切关注其产品动向。
4.4. Cellectis:通用型CAR-T,领域革新
CAR-T疗法目前还属于个性化治疗,需要对每个病人进行特定的设计治疗方案,因此造成治疗价格过高和疗效不确定性。尤其是疗效的不确定性,可能在某些患者身上能够完全缓解,而在另一些患者身上却毫无反应。这是由于来自不同的病人,每批 T 细胞的质量参差不齐,其他科学和生产变量的不同(如嵌入外来 DNA 所用的载体、细胞培养技术、运输及回输到患者体内的时机、选择的化疗方案等)均会使结果难以预料。
Cellectis 开发了一款“通用型”CAR-T疗法,UCART123,与传统CAR-T疗法需要定制化改造患者自体的T细胞不同,UCART123可以对异体T细胞进行提前制备,直接提供给患者使用。今年2月,UCART123成为首款经过FDA批准进入临床试验的通用型CAR-T疗法。
然而,UCART123在后续试验过程中,出现一名患者不幸死亡的情况,使得FDA在9月4日决定暂停这项试验,要求Cellectis公司对UCART123在安全性上做重新设计。在和FDA进行商讨后,Cellectis决定对UCART123的临床1期试验进行一系列的改动。2017年11月6日,Cellectis公司宣布,FDA允许其在研产品异体CAR-T细胞疗法(UCART123)的临床试验继续进行。UCART123目前正在积极开展治疗急性骨髓性白血病(AML)及母细胞性浆细胞样树突细胞肿瘤(BPDCN)的临床试验。
今年是CAR-T疗法的元年,目前已经有两款CAR-T疗法的上市。如果通用型CAR-T疗法能够顺利问世,对于患者来说又多了一条全新的治疗方案。而且,如果异体CAR-T最终可行,单例治疗价格有望大幅下降,生产效率也会大幅提升,CAR-T治疗领域也将迎来重要变革。
5. 国内企业紧跟前沿,四大逻辑筛选优秀企业
中国此次紧紧的把握住这一时代潮流,研发项目全面布局。据美国Clinical Trials数据显示,目前来自中国登记开展的CAR-T临床研究项目151项,在数量上超过欧洲,仅次于美国。其中,安科生物、金斯瑞、科济生物、西比曼、复星医药、药明康德等公司都在积极布局CAR-T细胞治疗。从事CAR-T研究的公司集中于上海和北京,尤其是上海,集中了超过三分之一数量的企业,这些企业很多通过与国外巨头公司合作或大量引进海外资深科研人才,以促进CAR-T产业在国内的发展。
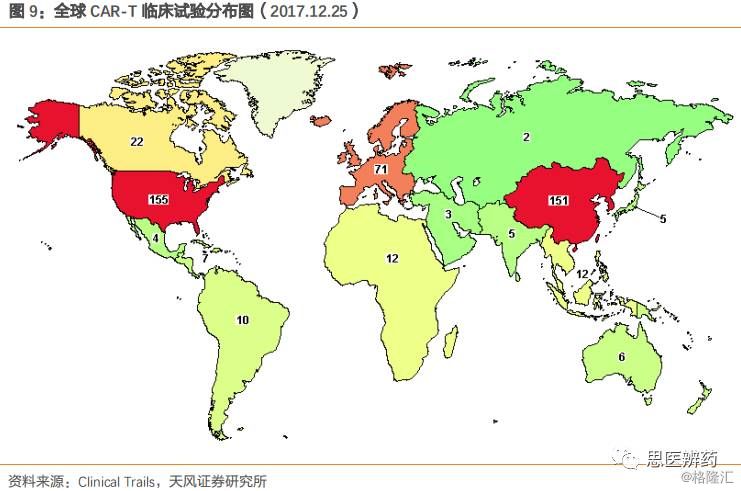
面对巨大的市场,国内众多的免疫细胞治疗公司,我们精选以下投资逻辑:
短期来看以主题投资为主,建议重点关注产品上市周期有望缩短的公司,从两个阶段进行考量,一个是前期开发阶段,另一个是临床试验阶段。中长期来看,将以业绩释放为核心关注点,重点关注两个方向,分别为具备成本优势的公司和布局新适应症方向的公司。我们建议从四条逻辑线筛选公司,并且根据以下逻辑筛选出具备潜力的优秀标的(排名不分先后):
1. 引进或开发与诺华、Kite获批产品具有相同或相似结构的产品
诺华和Kite获批产品在临床试验上具备令人满意的数据,Juno的失败同样也为后进入者提供了丰富的经验,节省大量时间和金钱的投入。国内已有大型企业与Kite、Juno建立合资公司(复星医药和Kite合作建立复星凯特公司,药明康德和Juno合作建立药明巨诺公司),将两家外企成熟的产品加速引入国内,由于Kite、Juno的产品早已在海外积累了丰富的经验,引入国内后有望通过成熟技术加速本土化应用,缩短开发周期,成功完成研发的概率更高。
此外,国内大量模仿诺华和Kite获批产品的靶点、共刺激结构域等设计,若能获得令人满意的临床试验数据,鉴于这两款产品在FDA成功获批的经历,这部分产品将减少试错时间成本,有望快速完成开发阶段,加入注册上市的竞争队列。
相关标的:复星凯特(复星医药)、药明巨诺(药明康德)
2. 具备大量理想的临床试验数据,有望缩短产品最终上市周期
在此次的《细胞治疗产品研究与评价技术指导原则》(试行)中,提及如果已有的人体数据在经过科学地评估后,则非临床研究可以本着具体品种具体分析的原则免除不必要的动物试验。另外,可以不同程度接受非注册临床试验数据,用于支持药品在中国的注册上市以及上市后安全有效性信息的更新。非注册临床试验数据的可接受程度取决于临床试验用样品与申报注册产品的一致性以及临床研究数据的产生过程,数据的真实性、完整性、准确性和可溯源性,以及CFDA对临床试验的核查结果等情况综合科学评价。由于细胞治疗产品的特殊性,将以两个阶段临床试验代替传统三期临床,并鼓励申报企业与CDE保持沟通确保方案设计合理性。
我们认为前期进行大量高质量的临床试验,充分总结经验,获得理想的试验数据,将可能在审评环节通过免除动物试验、采纳前期临床数据等方式加速流程,缩短时间,加快整体上市步伐。
相关标的:博生吉安科(安科生物)、南京传奇生物(金斯瑞)、西比曼
3. 具有规模化标准化生产流程、强大资金实力、丰富团队管理经验的成熟企业
企业需要具备成熟的细胞生产和转化医学研究平台,诺华获批的产品是与宾夕法尼亚大学合作研发的,宾夕法尼亚大学临床细胞和疫苗生产中心是符合FDA cGMP标准的细胞生产中心,是获得国际细胞治疗认证基金(FACT,由国际细胞治疗学会和美国血液和骨髓移植学会合办的非营利机构,负责细胞治疗领域的检查和认证)认证的GMP机构,设备齐全,自动化程度高,标准化流程,为CAR-T产品研发生产提供强大支持,通过标准化流程可以大幅缩短生产时间,降低成本,有望在未来上市竞争阶段领先对手,抢夺市场份额。
免疫细胞治疗产品前期科研投入巨大,尤其在临床阶段,企业需要有稳定的融资渠道,保证产品研发进程的顺利开展;
通过人才引进、高校合作、与国际三大巨头强强联合等方式,吸收先进的科研团队管理经验,在研发、生产、临床治疗、分析检测配合紧密,分工合作,奠定产品研发的基础。
相关标的:博生吉安科(安科生物)、复星凯特(复星医药)
4. 布局新靶点、新结构的产品
除了诺华、Kite获批CD19靶点,国内也有不少企业在新的靶点上进行深入研发,中国企业在此次CAT-T之争中紧跟全球的步伐,在某些方向甚至引领全球。对于这类型企业,我们认为有两方面利好:
有望获得优先审评审批,进入绿色通道,缩短审批周期
避免激烈的竞争,充分享受蓝海红利
2017年12月11日,南京传奇生物科技有限公司(金斯瑞子公司)提交CAR-T疗法LCAR-B38M临床申请获得CDE正式承办受理,并于同月18日,获准进入优先审评审批通道,加快产品审评速度。LCAR-B38M是靶向于BCMA的一款CAR-T疗法,不同于诺华和Kite的CD19,适应症为多发性骨髓瘤,LCAR-B38M临床试验入组患者40人,其中完全缓解患者24人(60%),部分缓解患者15人(37.5%),客观缓解率达到97.5%。
对于新靶点、新结构的开发研究,将突破新的适应症,参考Kite的Yescarta的发展路径,其适应症与Juno和诺华的不同,避开与两大厂商的正面竞争,寻找差异化路径。
相关标的:南京传奇生物(金斯瑞)、科济生物(佐力药业)
5.1. 博生吉安科(安科生物):研发储备丰富,进度国内领先
博生吉作为先行的国内免疫细胞疗法开发公司,主要业务为开发以CAR-T、CAR-NK、aAPCCTL和aAPCNK为核心的细胞治疗技术和抗体靶向药物。2015年6月,安科生物出资2,000万元与博生吉成立合资公司博生吉安科,专注于CAR-T细胞治疗技术研究及其商业化。
博生吉安科目前已经有多个CAR-T项目处于临床试验阶段,以CD19为靶点的CAR-T产品于2016年10月正式启动治疗成人难治复发B-ALL、B-NHL的临床试验,入组21名患者(NHL患者2名,B-ALL患者19名),临床实验结果理想,B-ALL患者的完全缓解率CR达到90%,2名NHL患者完全缓解率CR为100%,无1例因CAR-T细胞回输导致死亡的案例,仅2例出现神经毒性。
公司研发储备丰富,进度在国内处于领先位置。目前除了CD19靶点,另外还有3个靶点处于临床试验阶段。以CD7为靶点的CAR-NK,适应症为复发难治T-ALL,具有重要的临床意义,目前处于临床试验阶段,预计2019年申报IND。公司在实体肿瘤(肺癌、胰腺癌)也有布局,靶点为MUC1,是国际首例临床试验获得疗效,预计2019年IND。
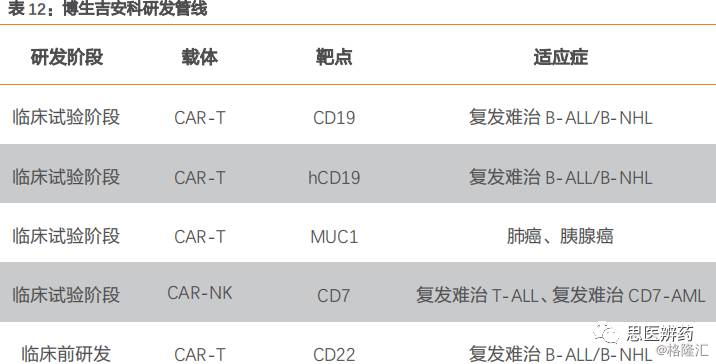

具备标准化流水线。公司具备全套GMP技术工艺,包括原材料准备中心和细胞制备中心,并且具备全流程质控流程,设立6大指控点,包含10余个QC指标,保证CAR-T制品高效和安全。根据前期临床试验积累的丰富经验,公司已建立起完善的细胞因子释放综合症CRS处理方案,保障患者的安全,避免重大事故的发生,达到理想的治疗效果。根据已有数据显示,博生吉安科的CAR-T产品在CRS致死、神经毒性、制备失败率等风险值上优于诺华、Kite、Juno同靶点产品,显示出其具有优秀的风险管控能力。
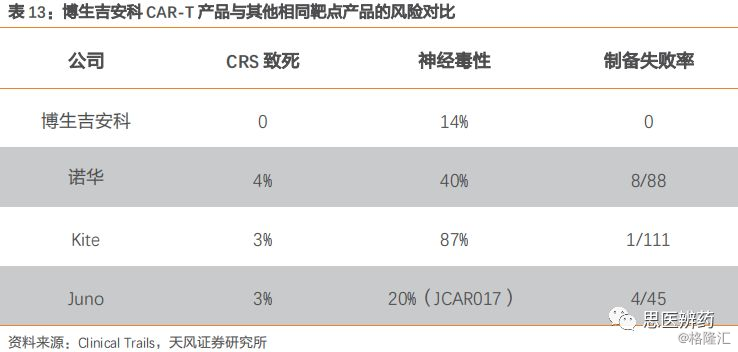
2016年10月27日安科生物公告,安科生物拟与参股子公司博生吉(参股20%)共同出资设立博生吉安科细胞技术有限公司,致力于特异性免疫细胞治疗技术和产品的产业化,同时合资公司独家享有特异性免疫细胞治疗技术专利的所有权,合作力度进一步加大。合资公司注册资本10,000万元,公司现金出资4,900万元,安科生物持有49%股权,公司还持有博生吉20%的股权,因此公司实际持有博生吉安科59.2%的股权。
5.2. 南京传奇生物(金斯瑞):新靶点新布局,CAR-T产品首获CDE受理
2017年 6月5日,在美国临床肿瘤学会年会上,南京传奇生物科技有限公司首席科学官范晓虎博士公布其针对多发性骨髓瘤自主研发的细胞疗法临床数据,引起业界的极大震动。公司于2016年3月起在国内进行早期临床试验,临床结果显示,35名既往治疗后复发的多发性骨髓瘤患者,接受治疗后病情客观缓解率达到100%,有5位观察期已超过一年,骨髓中检测不到癌细胞。85%的患者短期出现类似发热、肌痛、低血压等不良反应,但大多数症状轻微,一般治疗后两周之内恢复正常。截至2017年9月18日,南京传奇与中国4间医院合作临床研究及应用其自有CAR-T技术,已治疗71位患有复发难治的多发性骨髓瘤的病人。40位接受治疗的病人获跟进最少3个月,其中24位病人达到“完全反应”、12位达到“极好良好部分反应”、3位达到“部分反应”,针对复发难治的多发性骨髓瘤的病人客观缓解率达到97.5%。
在目前癌症治疗中,化疗客观缓解率大约为20%-30%,免疫系统药物最高的客观缓解率为30%-40%,即便是靶向药物,客观缓解率也只有70%-80%。南京传奇公司的技术对病情可达接近100%的客观缓解率,让多发性骨髓瘤患者看到被治愈的希望。多发性骨髓瘤是血液系统发病率第二的常见恶性肿瘤,目前无法完全治愈,病人每年为维持生命需花费数十万元。我国目前约有20万患者,每年还新增至少6万例,大多数患者生存期仅3-5年。
2017年12月11日,南京传奇生物科技有限公司提交CAR-T疗法中国临床申请(CXSL1700201)获得CDE正式承办受理,这是国内首个获得受理的CAR-T产品。
同月18日,药品评审中心CDE公布第二十五批优先审评审批名单,南京传奇生物的LCAR-B38M CAR-T细胞自体回输制剂获准进入优先审评审批通道,加快产品审评速度。
12月22日,强生旗下制药公司Janssen Biotech, Inc. 宣布与南京传奇生物签订合作协议,传奇生物将授予其关于LCAR-B38M的全球研发、生产和销售许可,与其专家团队共同研发并商业化LCAR-B38M,在海外地区,传奇生物与Janssen Biotech将采取费用和利润五五分成的方法,在国内,传奇生物将获得更大的利润空间,比例提高到70%。Janssen Biotech将一次性注入3.5亿美元用以支持研发,后续还将根据产品研发、生产、销售进度追加投资。
根据南京日报,南京传奇公司下一步计划在参与临床研究的4家中国医院招募100例病人,还计划2018年在美国开展类似临床试验,尽快把成果推向商业应用,造福患者。
5.3. 复星凯特(复星医药):引入成熟CAR-T产品,本土化落地事半功倍
2017年4月,复星医药和Kite Pharma在中国上海设立的合作企业,复星凯特生物科技有限公司,注册资本为4000万美元,致力于自主开发或转移世界最先进的细胞治疗技术,复星凯特建成了2000平方米的符合GMP标准,并且按照Kite设计标准要求的先进细胞生产工艺流程的洁净制备基地,为临床注册试验提供CAR-T细胞制剂。
复星凯特已获得Kite的CAR-T产品Yescarta在中国的全面技术转让和商业许可以推动此产品在中国的快速上市,后续两个正在开发的TCR产品也将在中国进行技术落地,开发、生产并使其商业化。同时,复星凯特也正在建立自主创新研发团队,致力于开发新型免疫细胞治疗产品,丰富公司的产品线,开拓更多适应症领域。
5.4. 科济生物(佐力药业):重点布局实体瘤,产品已获上海食药监受理
科济生物成立于2014年10月,主要进行对CAR-T细胞免疫治疗的研究,公司目前拥有大量在研项目,且大部分已处于临床一期阶段,其中包括全世界第一个针对肝细胞肝癌(HCC)以及针对多形性脑胶质瘤(GBM)临床研究,在2017年ASCO年会上,科济生物公布肝癌CAR-T一期临床结果,13名接受CAR-T细胞治疗的患难治复发的肝细胞癌患者均耐受良好,未出现剂量限制性毒性(DLT)或3级以上不良反应,下一步将开展全球Ib/II期临床试验,在已接受同样治疗方案的5名可进行疗效评估的患者中,1名患者出现部分缓解,2名疾病稳定,2名患者疾病进展。除一名疾病进展病人在治疗后12月死亡以外,其他4名病人都仍然存活,生存期已分别超过14个月、20个月、14个月和10个月。
12月11日,科济生物获得上海食药监《药品注册申请受理通知书》,其已经向上海市食品药品监督管理局递交了临床研究申请,上海食药监将联合相关单位出具意见之后,进一步向国家局申报。


2016年1月,佐力药业孙公司佐力创新医疗投资8,910万元增资科济生物,持有其7.85%的股权,成为公司第四大股东。本轮融资前的科济生物估值9.37亿元,融资完成后科济生物估值11.35亿元。
5.5. 西比曼:收购301医院CAR-T技术,多款产品已进入临床二期
2009年,西比曼生物科技(上海)有限公司(Cellular Biomedicine Group Ltd.)在中国成立,2014年正式在美国纳斯达克挂牌上市,成为唯一在美国纳斯达克上市的中国细胞生物医药科技公司。西比曼的CAR-T临床研究长期与解放军总医院(301医院)合作,2015年2月9日,收购了301医院的CAR-T细胞疗法,这项收购包括CD19、CD20、CD30、以及人表皮生长因子受体(EGFR)为靶点的免疫细胞治疗技术,已有的临床I/II期结果、相关专利的所有权、以及生产技术,并保留后续产品的优先收购权。
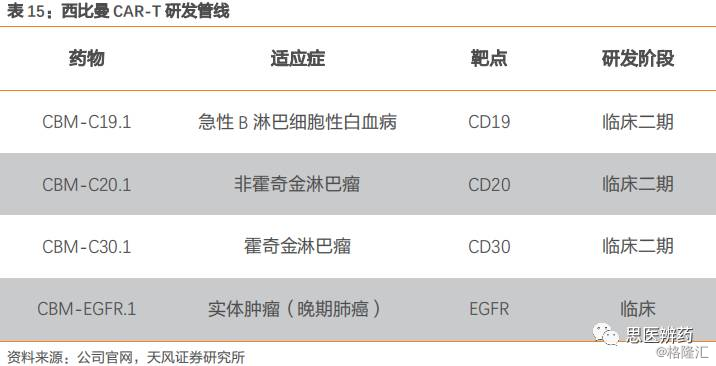
西比曼在CAR-T疗法的临床试验主要集中在临床二期,从目前公司公布的临床试验结果来看,初步显示这些产品相对安全、可行和有效。值得一提的是,其针对实体瘤EGFR靶点的CAR-T疗法CBM-EGFR.1的一期临床数据,在多种类型实体瘤上取得了应答,研发进度处于国际领先。
5.6. 冠昊生物:与北京大学强强联手,深度布局细胞治疗领域
在免疫细胞领域,公司引入邓宏魁教授团队,邓教授团队负责的CAR-T项目,在原有研究基础上开发了Tan-CAR技术,进一步解决CAR-T细胞在识别抗体时可能产生的逃逸现象。
公司与北京大学合作成立的北昊公司研发储备丰富,其中北昊公司控股的珠海泰赛尔细胞生物科技有限公司和北京军科正昊生物科技有限公司正在进行 CAR-T 项目技术研发和产业化。
6. CAR-T道路曲折,前途光明
目前,靶向CD19的CAR-T疗法在一些白血病和淋巴瘤中取得了成功,这为该疗法用于其它恶性肿瘤的治疗带来了福音。 同时我们也应注意到,CAR-T疗法在技术层面仍然面临着细胞因子释放综合症、神经毒性、脱靶效应等毒副作用以及实体瘤效果较差等问题,但是通过技术的不断优化改进,这些问题有望被缓解。
以最常见的细胞因子释放综合症为例,诺华的产品Kymriah获批上市时,FDA便将细胞因子释放综合症(CRS)列为 Kymriah的黑框警告,并提供一种对抗CRS的有效方案——罗氏的tocilizumab(托珠单抗,IL-6R单抗)。FDA同时也扩大批准了tocilizumab的适应症,用于对抗CAR-T疗法导致的严重细胞因子释放综合症。
对于较难解决的治疗流程的标准化问题,Cellectis 公司开发的UCART123“通用型”CAR-T疗法最近也被允许继续进行临床试验。
随着技术的不断进步,我们相信CAR-T治疗必将继续走向成熟。无论如何,CAR-T作为一种“活的靶向创新药”都称得上是一种革命性的疗法,并且有望使部分患有难治性肿瘤的患者获得持续的完全缓解。从商业化的角度来讲,CAR-T细胞疗法未来可能成为某些特定的复发性癌症的标准疗法,从而获得重磅炸弹级的销售额。
7. 风险提示
产品上市进度不达预期、产品研发失败、临床试验数据无法满足安全性有效性等要求、上市后产品销售不达预期、市场竞争激烈等。
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员



